|
||||||||||||||||||||||||
Государственное санитарно-эпидемиологическое
нормирование Российской Федерации
2.1.4. ПИТЬЕВАЯ ВОДА И ВОДОСНАБЖЕНИЕ
НАСЕЛЕННЫХ МЕСТ
Методические указания
по внедрению и применению
санитарно-эпидемиологических правил
и нормативов СанПиН 2.1.4.1116-02
«Питьевая вода. Гигиенические требования
к качеству воды, расфасованной в емкости.
Контроль качества»
Методические указания
МУ 2.1.4.1184-03
Минздрав России
Москва
Методические указания по внедрению и применению санитарных правил и нормативов СанПиН 2.1.4.1116-02 «Питьевая вода. Гигиенические требования к качеству воды, расфасованной в емкости. Контроль качества». МУ 2.1.4.1184-03. - М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2003.
1. Разработаны: НИИ экологии человека и гигиены окружающей среды им. А.Н. Сысина РАМН (академик РАМН Ю.А. Рахманин, д.м.н. Р.И. Михайлова, чл.-корр. РАМН Г.И. Красовский, проф., д.м.н. З.И. Жолдакова, к.т.н. Л.Ф. Кирьянова, к.м.н. И.Я. Рыжова, к.б.н. Е.М. Севостьянова, к.м.н. А.В. Алексеева, проф. д.м.н. B.C. Журков, к.м.н. Н.А. Егорова, к.м.н. О.Л. Синицына, к.м.н. А.Е. Недачин, к.м.н. Т.В. Доскина, к.м.н. Р.А. Дмитриева, к.б.н. Т.З. Артемова, к.б.н. Л.В. Иванова, к.м.н. Н.В. Чугунихина, к.б.н. Л.Г. Донерьян, к.б.н. Е.Е. Полякова, О.Ю. Киселева, А.Ю. Сковронский, А.А. Олесинов, Л.В. Ахалъцева), Московской медицинской академией им. И.М. Сеченова (проф. д.м.н. А.А. Королев, проф. д.м.н. М.В. Богданов), ИМП и ТМ им. Е.И. Марциновского ММА им. И.М. Сеченова Минздрава России (проф., д.м.н. Н.А. Романенко, к.м.н. Г.И. Новосильцев), Российской медицинской академией постдипломного образования (проф. д.м.н. В.Я. Голиков, О.Е. Тутельян), Смоленским государственным медицинским институтом МЗ РФ (д.м.н. А.В. Авчинников), Департаментом Госсанэпиднадзора Минздрава России (Л.П. Гульченко, И.Т. Ибрагимова), ВНИИ стандартизации (Борисов Н.П., Марина М.В., Бажанова Е.Б.).
2. Рекомендованы к утверждению Комиссией по госсанэпиднормированию при Минздраве России (прот. № 16 от 25.12.02).
3. Утверждены Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации Г.Г. Онищенко 15 января 2003 г.
4. Введены впервые.
СОДЕРЖАНИЕ
УТВЕРЖДАЮ
Главный государственный
санитарный врач Российской Федерации,
Первый заместитель Министра
здравоохранения Российской Федерации
Г. Г. Онищенко
15 января 2003 г.
Дата введения 1 апреля 2003 г.
2.1.4. ПИТЬЕВАЯ
ВОДА И ВОДОСНАБЖЕНИЕ
НАСЕЛЕННЫХ МЕСТ
Методические указания по внедрению и применению
Санитарно-эпидемиологических правил и нормативов
СанПиН 2.1.4.1116-02 «Питьевая вода. Гигиенические
требования к качеству воды, расфасованной в емкости.
Контроль качества»
Методические указания
МУ 2.1.4.1184-03
1. Общие положения
1.1. Настоящие методические указания (МУ) по внедрению санитарных правил и норм «Питьевая вода. Гигиенические требования к качеству воды, расфасованной в емкости. Контроль качества» (СанПиН 2.1.4.1116-02) предназначены для юридических лиц и индивидуальных предпринимателей (далее - изготовитель), деятельность которых связана с разработкой, производством, испытаниями и реализацией расфасованных питьевых вод, а также для органов и учреждений санитарно-эпидемиологической службы, осуществляющих государственный санитарно-эпидемиологический надзор, и испытательных центров (лабораторий), аккредитованных в области гигиенической оценки питьевой воды, расфасованной в емкости.
1.2. Основная задача МУ - обеспечить реализацию требований СанПиН 2.1.4.1116-02 (далее - СанПиН) в части производственного контроля за качеством питьевых вод, расфасованных в емкости (далее - расфасованных вод), и государственного санитарно-эпидемиологического надзора (ГСЭН) за данным видом продукции.
1.3. Выдачу санитарно-эпидемиологического заключения на расфасованную воду осуществляет Департамент ГСЭН Минздрава России (приказ МЗ РФ от 15.08.01 № 325) или аккредитованные центры ГСЭН. Срок действия санитарно-эпидемиологического заключения составляет 5 лет, на опытную партию - до 1 года.
1.4. В настоящих методических указаниях представлены:
• организационно-правовые аспекты СанПиН;
• основные особенности СанПиН;
• алгоритм гигиенической оценки воды водоисточника и расфасованной воды;
• принципы разработки рабочих программ производственного контроля за качеством расфасованных вод;
• требования к организации производственного контроля за качеством расфасованной воды.
Государственный санитарно-эпидемиологический надзор за организацией производства и качеством расфасованной питьевой воды.
2. Организационно-правовые аспекты СанПиН
2.1. Настоящие методические указания разработаны на основании Федерального закона «О санитарно-эпидемиологическом благополучии населения» от 30 марта 1999 г. № 52 ФЗ в соответствии с положением «О государственном санитарно-эпидемиологическом нормировании», утвержденном постановлением Правительства РФ от 24 июля 2000 г. № 554, а также положением «О санитарно-эпидемиологической экспертизе продукции», утвержденным приказом Министерства здравоохранения Российской Федерации от 15.08.01 № 325.
2.2. В соответствии с п. 3.1 СанПиН и согласно Федеральному закону «О санитарно-эпидемиологическом благополучии населения» к санитарно-эпидемиологическому надзору отнесена деятельность органов и санитарно-профилактических учреждений, направленная на обеспечение населения высококачественной физиологически полноценной питьевой водой и профилактику заболеваний людей, связанных с недостатком или избытком жизненно важных биогенных элементов.
2.3. Задачи производственного контроля качества расфасованных вод, обеспечиваемого изготовителем, определены требованиями СП 1.1.1058-01.
3. Необходимость разработки и основные особенности СанПиН «Питьевая вода. Гигиенические требования к качеству воды, расфасованной в емкости. Контроль качества»
3.1. Разработка и введение в действие СанПиН обусловлены отсутствием нормативной базы, регламентирующей требования к расфасованной воде, необходимостью гармонизации Российских нормативов с рекомендациями ВОЗ, ЕС, международной ассоциации бутылированной воды (IBWA), новыми научными знаниями о влиянии питьевой воды на здоровье населения, а также повсеместным ухудшением качества воды поверхностных и подземных водоисточников и ограниченной барьерной ролью традиционных технологий водоподготовки в отношении растворенных токсичных веществ.
3.2. Введение в действие СанПиН направлено на обеспечение доброкачественной питьевой водой, отвечающей современным гигиеническим требованиям, в т.ч. и по содержанию основных жизненно важных биогенных элементов (йод, фтор, кальций, магний, калий), широкого круга населения и, в первую очередь, групп населения, нуждающихся в укреплении здоровья (беременные женщины, дети, лица пожилого возраста, больные, страдающие заболеваниями почек и печени).
3.3. Требования настоящего СанПиН предусматривают использование питьевых вод с минерализацией не более 1000 мг/л, полученных из различных источников (подземные, поверхностные). В отличие от минеральных вод (лечебных и лечебно-столовых) расфасованные воды предназначены для питьевых целей и приготовления продуктов питания и в т.ч. в качестве единственного источника воды без неблагоприятных последствий для здоровья в течение всей жизни человека. Классификация расфасованных вод дана в приложении 1 настоящего документа.
3.4. Настоящий СанПиН, сохраняя преемственность гигиенических критериев СанПиН 2.1.4.1074-01, дополнен рядом новых критериев и положений.
3.4.1. Введены принципиально новые критерии оценки качества расфасованных вод: физиологическая полноценность по микро- и макроэлементному составу (в т.ч. с учетом норм суточного водопотребления), стабильность качества (сохранность питьевых свойств на протяжении срока хранения). Расширен перечень показателей и ужесточены нормативы, характеризующие безвредность химического состава и эпидемическую безопасность. Предусмотрено исключение вторичного загрязнения в результате миграции химических веществ из материала емкостей, конструкционных материалов, реагентов и дезинфектантов, используемых при водоподготовке исходной (сырьевой) воды.
3.4.2. Сформулированы основные принципы медикобиологической классификации качества расфасованных вод для определения категорий их качества.
3.4.3. Даны гигиенические нормативы для расфасованных вод в зависимости от категорий качества.
3.4.4. Указаны требования к показателям безвредности химического состава расфасованной воды и ее эпидемической безопасности с учетом сроков и температуры хранения, гармонизированные с требованиями ЕС, ВОЗ, IBWA.
4. Правила проведения гигиенической оценки исходных (сырьевых) и расфасованных вод
4.1. Целью гигиенической оценки расфасованной воды является обеспечение населения питьевой водой высокого качества, полностью отвечающей требованиям СанПиН.
4.2. Выдача санитарно-эпидемиологического заключения на расфасованную воду производится Департаментом ГСЭН МЗ РФ или аккредитованными центрами СЭН на основании экспертизы соответствующих документов и результатов исследований качества воды согласно методической схеме (таблица 1).
• заявку и сопроводительное письмо на проведение гигиенической оценки воды, предназначенной для промышленного розлива или уже расфасованной воды;
• протоколы исследований качества воды, выданные аккредитованными испытательными центрами;
• необходимую техническую и эксплуатационную документацию.
Таблица 1
Методическая схема проведения исследований по гигиенической оценке расфасованных вод
|
Основная цель |
Основные возможные результаты |
|
|
1. Анализ исходной документации на производство расфасованной воды, в т.ч. и гигиеническая экспертиза оборудования, потребительской тары, материалов, веществ, в т.ч. минеральных добавок, используемых при производстве и розливе воды |
Определение объема и последовательности необходимых исследований |
Экспертиза представленной документации. Гигиеническая оценка только готовой продукции по заявленным срокам хранения. Исследование в полном объеме по методической схеме (этапы II - V) |
|
II. Гигиеническая оценка исходной (сырьевой) воды из водоисточника |
Санитарно-эпидемиологическое заключение на воду водоисточника |
Несоответствие необходимым требованиям СанПиН с рекомендациями по технологии водоподготовки (кондиционирования). Полное соответствие одной из категорий качества. Рекомендации по технологии для перевода воды в более высокую категорию качества |
|
III. Гигиеническое исследование новых материалов и веществ, используемых при производстве и розливе воды |
Гигиеническая оценка новых материалов и веществ |
Положительная гигиеническая оценка с выдачей санитарно-эпидемиологического заключения на новые материалы и вещества и включением их в «Перечень» разрешенных реагентов и материалов. Отрицательная оценка, рекомендации по адекватной замене на разрешенные реагенты и материалы |
|
IV. Гигиеническое изучение динамики качества расфасованной воды при различных условиях и сроках ее хранения |
Гигиеническая регламентация условий хранения и сроков реализации расфасованных вод |
Универсальная характеристика продукции: срок хранения от 3 до 12 мес. (в зависимости от вида продукции) при трех температурных режимах. Ограничение условий хранения и сроков реализации продукции |
|
V. Оформление санитарно-эпидемиологического заключения на расфасованные воды и установление категории качества расфасованной воды* |
Санитарно-эпидемиологическое заключение по расфасованным водам (готовой продукции) |
Получение санитарно-эпидемиологического заключения на опытную партию (на срок 1 год). Получение санитарно-эпидемиологического заключения на серийно выпускаемую продукцию (на срок 5 лет). Дополнительная экспертиза по специальным вопросам |
|
* При наличии в производстве расфасованной питьевой воды новых материалов и реагентов, используемых для ее обработки и расфасовки, заказчик обеспечивает проведение необходимых гигиенических (а если требуется и санитарно-токсикологических) исследований в соответствии с МУ 2.1.4.783-99 «Гигиеническая оценка материалов, реагентов, оборудования, технологий, используемых в системах водоснабжения» для решения вопроса о включении данных материалов и реагентов в «Перечень разрешенных материалов и реагентов для применения в практике хозяйственно-питьевого водоснабжения», утвержденный Департаментом ГСЭН МЗ РФ. |
||
• паспорт на скважину;
• разрешение на водопользование;
• заключение территориального центра ГСЭН о санитарно-эпидемической надежности водоисточника - на основании ГОСТ 2761 «Источники централизованного хозяйственно-питьевого водоснабжения» и СП 2.1.5.1059-01 «Гигиенические требования к охране подземных вод от загрязнения». В случае использования воды централизованных систем водоснабжения качество исходной (сырьевой) воды должно соответствовать требованиям действующего СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества»;
• протоколы исследований качества воды (по сезонам) за период наблюдения;
• протоколы углубленных физико-химических, микробиологических, паразитологических, радиологических исследований и экспресс-токсикологического (биотестирования) анализа воды, выполненных в соответствии с перечнем показателей, представленных в приложении 2;
• заключение аккредитованного испытательного Центра (лаборатории).
4.3.2. При гигиенической оценке исходной (сырьевой) питьевой воды (из подземных водоисточников), предназначенной для розлива в бутыли после ее кондиционирования с использованием специальных технологий доведения отдельных показателей качества воды до необходимых гигиенических требований, дополнительно к документам, указанным в п. 4.3.1, представляются:
• технологический регламент (технологическое описание, технологическая инструкция), согласованный аккредитованным центром ГСЭН;
• Санитарно-эпидемиологические заключения на материалы, в т.ч. минеральные компоненты и оборудование, используемые при производстве и розливе расфасованной воды*.
* Для продукции, поступающей по импорту, представляется сертификат безопасности, выданный уполномоченным органом страны-экспортера на языке страны и в переводе на русский, официально заверенном.
4.3.3. При гигиенической оценке исходной («сырьевой») водопроводной воды, получаемой из поверхностного водоисточника и предназначенной для розлива в емкости после ее кондиционирования с использованием специальных технологий доведения отдельных показателей качества воды до необходимых гигиенических требований, предоставляются документы, аналогичные указанным в пп. 4.3.1 и 4.3.2, но вместо паспорта на скважину представляется заключение территориального центра ГСЭН о степени защищенности и постоянства состава воды водоисточника в месте водозабора.
4.3.4. При гигиенической оценке расфасованной воды предоставляются:
• технические условия, утвержденные в установленном порядке;
• технологический регламент (технологическое описание, технологическая инструкция), согласованный территориальным центром ГСЭН;
• протоколы углубленных физико-химических., микробиологических, паразитологических, радиологических исследований и экспресс-токсикологического анализа сырьевой воды, выполненных в соответствии с перечнем показателей, представленных в приложении 2;
• санитарно-эпидемиологическое заключение на материал емкостей для розлива воды или название материала, из которого изготовлена емкость; протоколы исследований качества расфасованной воды в течение гарантийного срока хранения при температурах 4 °С; 20 - 22 °С и 37 °С с указанием регламентированных сроков и условий хранения (приложение 3);
• этикетку с указанием наименования, вида, типа и категории расфасованной воды, данных анализа о ее химическом составе (уровень общей минерализации; содержание основных макро- и микроэлементов: кальций, магний, калий, натрий, хлориды, нитраты, сульфаты, бикарбонаты, фториды и т.д.), номинальный объем воды в упаковке в литрах, указания по применению, срок годности, условия хранения, информацию о сертификации;
• общие требования к информации для потребителя - по ГОСТ Р 51074;
• заключение испытательной лаборатории по результатам гигиенической оценки и экспертизы расфасованной воды с обоснованием категории ее качества.
4.4. Органы и учреждения государственной санитарно-эпидемиологической службы, как орган выдачи санитарно-эпидемиологического заключения:
• направляет представленные Изготовителем документы для их всесторонней экспертизы в Испытательные центры, аккредитованные в установленном порядке на право проведения санитарно-эпидемиологических экспертиз;
• рассмотрев представленные документы и результаты указанной экспертизы в срок - не позднее 1 месяца, сообщает Изготовителю свое решение:
а) о выдаче санитарно-эпидемиологического заключения на расфасованную воду при полном соответствии представленных документов необходимым требованиям;
б) решение о проведении испытаний в полном объеме, что отражается в соответствующем документе;
в) решение о сокращении объема, при повторных испытаниях (для продления срока действия санитарно-эпидемиологического заключения).
При отсутствии у Изготовителя необходимой документации или ее части обеспечивает взаимодействие Изготовителя с Испытательным центром с целью проведения необходимых гигиенических исследований в соответствии с п. 4.3.
4.4.2. Присвоение расфасованным водам высшей категории качества проводится с учетом требований п. 4.4.1 при обязательном согласовании с Департаментом ГСЭН МЗ РФ.
4.4.3. Заказчик, в случае несогласия с выданным санитарно-эпидемиологическим заключением, может обратиться с апелляцией в Совет руководителей испытательных центров, созданный приказом Министра здравоохранения «О совете руководителей испытательных центров» РФ № 21/71 от 14.07.00 при Министерстве здравоохранения Российской Федерации.
4.5. Испытательный центр осуществляет:
• отбор проб воды для соответствующих испытаний или согласование его с другой компетентной организацией;
• проведение исследований по гигиенической оценке расфасованных вод в соответствии с методической схемой (таблица 1), в сроки, установленные договором с Изготовителем.
При отборе проб воды для проведения испытаний должна быть обеспечена их полная идентичность с серийной продукцией, поставляемой изготовителем (заказчиком), в отношении исходных материалов, сырья, технологий производства и других факторов, которые могут влиять на качество данной продукции.
В зависимости от полноты исследований и оцениваемой продукции отбор проб проводится с учетом данных приложения 4.
4.5.1. Гигиеническая оценка качества расфасованных вод проводится с использованием современных методов исследования (приложение 5), путем достоверной оценки ее соответствия основным и дополнительным гигиеническим требованиям по эпидемической и радиационной безопасности, безвредности химического состава, благоприятности (привлекательности) органолептических свойств, физиологической полноценности по макро- и микроэлементному составу, стабильности качества на весь период целевого использования.
4.5.2. В зависимости от исходных полимерных материалов и технологических режимов, применяемых для изготовления тары, использования возвратной тары, «агрессивности» расфасованных вод гигиенические исследования должны включать дополнительные показатели, связанные с возможной миграцией в воду химических веществ, в т.ч. входящих в рецептуру полимерного материала потребительской тары (приложение 6).
4.5.3. В заключении Испытательного центра (лаборатории) могут даваться рекомендации на основе дополнительной экспертизы по специальным вопросам (п. 5, табл. 1), в частности рекомендации по кондиционированию биологически активными эссенциальными элементами (йод, фтор) на основе данных оценки суммарного поступления в организм указанных микроэлементов из всех объектов окружающей среды с учетом допустимой суточной дозы.
5. Организация производственного контроля за качеством расфасованных вод
5.1. Основные требования к организации производственного контроля качества расфасованной питьевой воды установлены в разделе 6 СанПиН.
5.2. Выбор контролируемых показателей, подлежащих постоянному производственному контролю, проводится в процессе разработки рабочей программы производственного контроля за качеством питьевой воды.
5.3. Рабочая программа производственного контроля включает: пояснительную записку, перечень контролируемых показателей, перечень методик их определения, правила приемки готовой продукции, перечень должностных лиц, на которых возложены функции по осуществлению производственного контроля, перечень должностных лиц, подлежащих медицинским осмотрам, профессиональной гигиенической подготовке.
5.4. Пояснительная записка должна содержать: информацию о готовой продукции и санитарно-эпидемиологическое заключение на нее, сведения, характеризующие источник воды, используемой для розлива (поверхностный, подземный, водопроводная вода централизованных систем водоснабжения из подземного или поверхностного водоисточника) и санитарно-эпидемиологическое заключение на него (кроме воды централизованного хозяйственно-питьевого водоснабжения), технологию водоподготовки и санитарно-эпидемиологическое заключение на нее, перечень реагентов и материалов, используемых в водоподготовке и санитарно-эпидемиологические заключения на них, характеристику емкостей и укупорочных средств и санитарно-эпидемиологическое заключение на них. В пояснительной записке указывают также готовность производственной лаборатории к проведению контрольных работ, план мероприятий по улучшению технологии водоподготовки, план ликвидации аварийных ситуаций и системы оповещения учреждений ГСЭН и населения.
5.5. В порядке производственного контроля на предприятиях по производству расфасованных вод должно контролироваться:
• качество расфасованной воды;
• качество воды водоисточника;
• качество воды по этапам водоподготовки;
• качество реагентов, используемых при водоподготовке;
• соблюдение санитарных требований к емкостям и укупорочным изделиям;
• соблюдение технологических параметров, режимов обеззараживания, установленных в технологической документации;
• соблюдение мер по обеспечению безопасности труда персонала.
5.6. В каждой партии готовой продукции обязательному контролю подлежат следующие показатели:
• органолептические (запах, привкус, цветность, водородный показатель);
• микробиологические (ОМЧ при 37 °С; ОКБ; ГКБ);
• содержание реагентов, используемых для консервации и обеззараживания.
5.6.1. Определение ОМЧ при 22° и 37 °С проводят по методу, указанному в приложении 7.
5.6.2. Определение общих и глюкозоположительных колиформных бактерий (ОКБ и ГКБ) проводят ускоренным методом (приложение 8).
5.7. При периодическом анализе готовой продукции (не реже одного раза в месяц) дополнительно к контролируемым показателям, указанным в п. 5.6, проводят контроль по следующим показателям:
• органолептические (мутность);
• обобщенный (перманганатная окисляемость);
• микробиологические (ОМЧ при 22 °С, Pseudomonas aeruginosa).
5.7.1. Определение Pseudomonas aeruginosa в готовой продукции проводят в аккредитованных центром ГСЭН лабораториях (приложение 9).
5.8. Полный анализ качества расфасованной воды на соответствие требованиям СанПиН (таблицы 1 - 6) и другой нормативной документации проводится не реже одного раза в год в аккредитованных центром ГСЭН лабораториях в соответствии с методами, указанными в приложениях 5 - 11.
5.8.1. Определение колифагов проводят по методу, указанному в приложении 10.
5.8.2. Определение ооцист криптоспоридий проводят по методу, указанному в приложении 11.
5.9. В рабочую программу включают перечень методик определения контролируемых показателей с указанием информации о методе - шифр ГОСТ или РД, предел и погрешность определения (приложение 5).
5.10. Для проведения лабораторных исследований (измерений) качества расфасованной воды допускаются метрологически аттестованные методики, соответствующие требованиям ГОСТ 8.563 и ГОСТ 8.566, установленные значения показателей и погрешности которых не превышают норм погрешности по ГОСТ 27384. Погрешность микробиологических методов устанавливается в соответствии с методиками, разрешенными к применению Минздравом России.
5.11. Отбор проб, условия транспортирования и сроки хранения проб должны соответствовать требованиям ГОСТ Р 51592 и по ГОСТ Р 51593.
5.12. Правила приемки готовой продукции определены ГОСТ 23268.0.
5.13. Схема бактериологического контроля качества расфасованных вод и по этапам водоподготовки приведена в приложении 12.
Рекомендуемая в приложении 8 минимальная частота отбора проб может быть увеличена в период налаживания производства, а также при необходимости повышения надежности контроля, в зависимости от особенностей производства, в условиях неблагоприятной эпидемической ситуации и т.п.
На производствах, которые выпускают менее 100 бутылок в день, объем контроля может быть снижен по согласованию с территориальным центром ГСЭН.
5.14. Контроль технологического режима по этапам водоподготовки (фильтрации, обезжелезивания, обессоливания, сорбции, кондиционирования макро- и микроэлементного состава, обеззараживания, консервирования и др.) должен проводиться по соответствующим показателям не реже одного раза в смену.
5.15. Повышенное насыщение расфасованной воды двуокисью углерода (свыше 0,4 %) с целью придания ей свойств напитка (сильно газированная питьевая вода) допустимо при условии обязательного указания на этикетке содержания двуокиси углерода и строгом контроле качества используемого консерванта требованиям ГОСТ 8050.
5.16. Партия продукции может поступить в реализацию только после получения результатов бактериологического анализа, поэтому при выполнении сокращенного анализа допустимо использование ускоренных методов (приложение 8).
Допустимо использовать коммерческие питательные среды и системы идентификации, предназначенные для выполнения регламентируемых СанПиН показателей. Питательные среды, системы и другие препараты зарубежного производства должны иметь международный сертификат качества ISO 9000 или EN 29000.
5.17. При несоответствии результатов лабораторных исследований расфасованных вод гигиеническим требованиям повторно исследуют удвоенное количество их образцов, а также проводят санитарно-гигиеническое расследование для выявления причин такого несоответствия. После проведения соответствующих мероприятий должен быть осуществлен контроль их эффективности.
Если неудовлетворительный результат получают по показателю ОМЧ, то анализ на Pseudomonas aeruginosa обязателен.
5.18. При получении неудовлетворительных результатов лабораторных исследований качества готовой продукции на удвоенном количестве образцов партия бракуется и подлежит снятию с реализации вся партия. Изготовитель расфасованных питьевых вод совместно с территориальным центром ГСЭН разрабатывает и проводит необходимые санитарно-гигиенические и противоэпидемические мероприятия. Любые оперативные решения по запрещению использования расфасованных вод населением принимаются по согласованию с территориальным центром ГСЭН, трактовка степени опасности расфасованных вод дается учреждениями ГСЭН.
5.19. При выборе мест отбора проб для бактериологического анализа руководствуются необходимостью контроля каждого критического узла, где возможно изменение качества воды: исходная вода, поступающая на производство; накопительные резервуары до водоподготовки; на каждом этапе водоподготовки; перед розливом, если обеззараживание проводят не на заключительном этапе; готовая продукция с каждой линии. Эпидемическую опасность представляют оголовок скважины (при автономном водозаборе), накопительные резервуары при хранении в них воды свыше 2 - 3 суток, соединительные шланги или фланцы на трубопроводах, фильтры любой конструкции, мембраны обратного осмоса и др., где возможно биообрастание, вторичное микробное загрязнение, размножение бактерий, в т.ч. патогенных и условно-патогенных.
5.20. Исследования питьевой воды на содержание патогенных микроорганизмов проводят исходя из эпидемической ситуации. Необходимость проведения этих исследований устанавливают и осуществляют выполнение анализов учреждения ГСЭН или другие лаборатории, аккредитованные в системе ГСЭН.
5.21. При возвратном цикле обязательному бактериологическому и органолептическому (запах, видимые пленки и другие включения и т.п.) контролю подлежат емкости перед розливом и укупорочные изделия в соответствии с приложением 13.
5.22. На предприятиях, где используют возвратные емкости, их мойку и стерилизацию должны осуществлять в автоматических моющих машинах. Мойку емкостей в автоматических моющих машинах следует производить в соответствии с инструкцией завода-изготовителя по их эксплуатации. Для мытья возвратных емкостей можно применять только моющие средства, разрешенные для пищевой промышленности, имеющие санитарно-эпидемиологическое заключение и сертификат соответствия.
5.23. При использовании для мойки возвратных емкостей автоматических машин обязательному контролю подлежат рабочая концентрация моющего средства и температура раствора, которые должны соответствовать рекомендациям производителя. Чистку и обеззараживание моющих машин выполняют по мере необходимости, но не реже 2 раз в неделю.
При ручной мойке емкостей раствор в ванне следует менять не реже 2 раз в смену. Контроль осуществляют в начале смены и затем через каждые 2 часа.
5.24. Контролю подлежат остаточное количество моющих средств (приложение 14) и дезинфектанта в случае его использования. Результаты технического и лабораторного контроля регистрируют в журнале.
5.25. Обеззараживание возвратных емкостей проводят в случаях, когда вода перед розливом не обеззараживается.
5.26. В рамках производственного контроля, проводимого изготовителем, обязательному контролю подлежит вода в местах водозабора.
5.27. Количество и периодичность проб воды в местах водозабора, отбираемых для лабораторных исследований, устанавливаются с учетом требований, указанных в СанПиН 2.1.4.1074-01.
5.28. При выборе показателей, контролируемых в водоисточнике, прежде всего используют базовую информацию, имеющуюся в организациях, контролирующих или изучавших качество воды источника посезонно, условия, формирующие качество воды водоисточника и т.д. Из указанных в приложении 3 обобщенных показателей в обязательном порядке определяют водородный показатель и перманганатную окисляемость. Другие химические вещества включают в рабочую программу в тех случаях, если по данным мониторинга установлено или прогнозируется их присутствие в водоисточнике. В исследованиях применяются методы контроля, указанные в приложении 5.
5.29. Срок действия утвержденных рабочих программ - не более 3 лет. При необходимости (в зависимости от изменившейся санитарной ситуации) он может быть сокращен.
6. Организация работы производственных лабораторий
6.1. Согласно СанПиН производственный контроль осуществляется предприятием, в структуре которого должна быть организована и аккредитована производственная лаборатория для выполнения химического и микробиологического анализа. При отсутствии производственной лаборатории анализы воды в соответствии с рабочей программой выполняются на договорной основе лабораторией, аккредитованной на проведение подобного рода деятельности.
6.2. При создании производственной лаборатории необходимо обеспечить:
• материальную базу (отдельные помещения, приборы, посуда, реактивы, питательные среды, аттестованные методики, ГСО, методическая документация и т.п.);
• метрологический контроль оборудования;
• технику безопасности работ, в т.ч. с микроорганизмами IV группы патогенности;
• штат специалистов надлежащей квалификации, имеющих документ об обучении методам проведения анализа.
Размещение бактериологической лаборатории в одном помещении с производственными линиями водоподготовки категорически запрещается.
6.3. Производственная лаборатория, где выполняют микробиологические анализы, должна получить разрешение территориальных центров ГСЭН на работу с микроорганизмами IV группы патогенности.
6.4. Государственный надзор за метрологическим обеспечением производственных лабораторий осуществляют территориальные органы Госстандарта России в установленном порядке.
6.5. Результаты исследований должны фиксироваться в лабораторных журналах (прошнурованных и опечатанных) и подписываться исполнителями анализов.
7. Государственный санитарно-эпидемиологический надзор за организацией производства и качеством расфасованной питьевой воды
7.1. Территориальные центры Государственного санитарно-эпидемиологического надзора осуществляют согласование проектов предприятий по производству расфасованных питьевых вод.
7.2. Для согласования производства на стадии проектирования должны быть предоставлены материалы:
• санитарно-эпидемиологическое заключение на водоисточник;
• обоснование технологической схемы водоподготовки;
• обоснование технологии подготовки тары и укупорочного материала.
7.3. Государственный санитарно-эпидемиологический надзор за организацией производства и качеством питьевых вод, расфасованных в емкости, включает:
• контроль за соблюдением ТУ;
• согласование технологий водоподготовки питьевых вод, программ производственного контроля (показатели, кратность и точки отбора проб, методы определения);
• регулярную оценку полноты и достоверности результатов, полученных в процессе производственного контроля;
• выборочный лабораторный контроль готовой продукции по программе и в установленные сроки;
• текущий санитарный контроль готовой продукции в торговых точках.
7.4. При анализе данных, полученных из производственных лабораторий и центров ГСЭН, обращают внимание на:
• соответствие результатов нормативным требованиям;
• степень совпадения результатов анализа производственной лаборатории и лаборатории центров ГСЭН.
7.5. При ухудшении санитарно-эпидемиологической обстановки в районе водозаборов и местах расположения предприятий центры ГСЭН совместно с изготовителем корректируют рабочую программу производственного контроля с увеличением частоты отбора проб, расширением спектра показателей.
7.6. В порядке государственного надзора центры ГСЭН проверяют ведение документации по регистрации результатов анализов по согласованным точкам и показателям, технологических параметров обеззараживания и т.д.
7.7. Текущий санитарный контроль готовой продукции, отбираемой в торговых точках, проводится по следующим основным показателям:
• органолептические (запах, цветность, мутность, рН);
• макроэлементный состав (жесткость, щелочность, хлориды, сульфаты, нитраты);
• тяжелые металлы (кадмий, свинец, ртуть, мышьяк);
• органические вещества (перманганатная окисляемость, хлороформ);
• микробный состав (ОМЧ при 37 °С, общие и глюкозоположительные бактерии, колифаги);
• дополнительные показатели, указанные на этикетке. Например: серебро, фтор, йод и т.д.
7.7.1. Результаты выборочного анализа готовой продукции (в случае несоответствия их нормативной документации) являются основанием для принятия соответствующих решений (проведение углубленного анализа расфасованной воды, запрещение реализации ее населению).
8. Термины и определения
ВОЗ - Всемирная Организация Здравоохранения при ООН.
ЕС - Европейское Сообщество.
IBWA - Международная ассоциация производителей бутылированной воды.
Допустимая суточная доза (ДСД) - количество вещества, поступающее в организм человека из всех сред в пересчете на массу тела (мг/кг массы тела), которое может потребляться ежедневно на протяжении всей жизни без заметного риска для здоровья.
Технические условия (ТУ) - нормативный документ, позволяющий идентифицировать данную продукцию. В ТУ отражаются назначение продукции, ее качественные показатели, правила приемки, методы контроля, условия транспортирования и хранения, гарантии изготовителя.
Технологический регламент (ТР) на систему водоподготовки «сырьевой» воды включает технологическую схему процесса водоподготовки (оборудование, способы и режимы эксплуатации и регенерации, перечень конструкционных материалов, реагентов, сорбентов, дезинфектантов, применяемых в технологии водоподготовки, а также материал упаковочной тары, с соответствующей к ним нормативной документацией (ТУ, ГОСТ, гигиенические заключения).
Общие колиформные бактерии (ОКБ) - интегральный показатель фекального загрязнения, который включает термотолерантные колиформные бактерии и Е. coli, и поэтому обладает более высокой индикаторной надежностью в отношении возбудителей бактериальных кишечных инфекций, распространяемых водным путем. Обнаружение ОКБ в воде свидетельствует о ее фекальном загрязнении, что указывает на потенциальную эпидемическую опасность и возможное попадание этим же путем возбудителей кишечных инфекций. Обнаруженный количественный уровень ОКБ позволяет судить о степени эпидемической опасности и, следовательно, экстренности проведения профилактических мероприятий.
Санитарно-показательная группа глюкозоположителъных колиформных бактерий (ГКБ) объединяет помимо ОКБ и ТКБ еще и лактозоотрицательные бактерии семейства Enterobacteriaceae по основному признаку этого семейства - ферментации глюкозы и является наиболее строгим бактериологическим показателем, что соответствует требованиям статьи 5 Директив ЕС 1998. В связи с этим показатель отличается гигиенической надежностью и чувствительностью, позволяя контролировать отсутствие в воде не только индикаторных, но и патогенных и условно-патогенных бактерий семейства Enterobacteriaceae.
Общее число микроорганизмов (ОМЧ), образующих колонии на питательном агаре при температуре 37 °С и при температуре 22 °С, включает разнообразные группы микроорганизмов и позволяет выявить не только фекальное загрязнение воды, но обусловленное другими источниками. Группа ОМЧ при температуре 37 °С в большей мере выявляет антропогенное микробное загрязнение; группа ОМЧ при температуре 22 °С является чувствительным индикатором вторичного загрязнения. Входящие в эту группу микроорганизмы, являясь гетеротрофами, косвенно указывают на наличие в воде легко усвояемых органических веществ, на неблагоприятное санитарное состояние систем хранения и подачи воды. Превышение нормативов, установленных в таблице 4 по показателям ОМЧ свидетельствует также о создании условий для размножения микроорганизмов. При этом накопление биомассы может способствовать размножению не только индикаторных, но и патогенных бактерий (например, сальмонелл), что представляет уже прямую эпидемическую опасность при использовании воды.
Pseudomonas aeruginosa относится к условно-патогенным микроорганизмам при водном пути передачи, поскольку может инфицировать людей с ослабленными защитными функциями. Pseudomonas aeruginosa в расфасованных водах представляет опасность вследствие способности к интенсивному размножению в водной среде, бедной органическими веществами, и при благоприятной температуре.
Колифаги - бактериальные вирусы, способные лизировать кишечную палочку и формировать зоны лизиса (бляшки) через 18 ± 2 ч при температуре 37 ± 1 °С на ее газоне на питательном агаре. Введены в качестве индикаторов более устойчивого к факторам окружающей среды вирусного загрязнения.
9. Библиографические данные
1. Федеральный закон «О радиационной безопасности населения» № 3-ФЗ от 09.01.96.
2. Закон Российской Федерации «О сертификации продукции и услуг» № 5151-1 от 10.06.93.
3. Закон Российской Федерации «О защите прав потребителей» № 2300-1 от 07.02.92.
4. Федеральный закон «О качестве и безопасности пищевых продуктов» № 29-ФЗ от 02.01.00.
5. Приказ МЗ РФ «О сертификации бытовых водоочистных устройств и бутылированной питьевой воды» № 47/24 от 24.03.94.
6. Приказ МЗ РФ «О гигиенической оценке производства, поставки и реализации продукции и товаров» № 217 от 20.07.98.
7. Приказ МЗ РФ «О совете руководителей испытательных центров» № 271 от 14.07.00.
8. Guidelines for drinking-water quality. Second edition. Volume Recommendations. - World Health Organisation. - Geneva, 1993.
9. Санитарные правила и нормы «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. СанПиН 2.1.4.1074-01».
10. Гигиенические нормативы «Нормы радиационной безопасности (НРБ-99). СП 2.6.1.758-99».
11. ГОСТ 2761-84. «Источники централизованного хозяйственно-питьевого водоснабжения. Гигиенические, технические требования и правила выбора».
12. Санитарные правила и нормы «Зоны санитарной охраны источников водоснабжения и водопроводов питьевого назначения. СанПиН 2.1.4.1110-02».
13. Санитарные правила «Гигиенические требования к охране подземных вод от загрязнения. СП 2.1.5.1059-01».
14. «Санитарные правила для предприятий по обработке и розливу питьевых минеральных вод» № 4416-87.
15. Методические указания «Гигиеническая оценка материалов, реагентов, оборудования, технологий, используемых в системах водоснабжения. МУ 2.1.4.783-99».
16. «Перечень материалов, реагентов и малогабаритных очистных устройств, разрешенных Государственным комитетом санэпиднадзора РФ для применения в практике хозяйственно-питьевого водоснабжения» № 01 - 19/32-11.
17. Методические рекомендации «Радиационный контроль питьевой воды» № 11-2/42-09, утв. Зам. Гл. сан. врача 04.04.00.
18. Справочник «Нормативное обеспечение контроля качества воды» (Госстандарт РФ. М., 1995).
19. ГОСТ 8050-85. «Двуокись углерода газообразная и жидкая. Технические условия».
20. ГОСТ 51074-97. «Продукты пищевые. Информация для потребителя. Общие требования».
21. ГОСТ Р 51153-98. «Напитки безалкогольные газированные и напитки из хлебного сырья. Метод определения двуокиси углерода».
22. ГОСТ Р 51232-98. «Вода питьевая. Общие требования к организации и методам контроля».
23. ГОСТ Р 51074-99. «Упаковка. Маркировка, указывающая на способ обращения с грузами».
24. ГОСТ Р, регистр. № РОСС RU.00.11 «Система сертификации питьевой воды, материалов, технологических процессов и оборудования, применяемых в питьевом водоснабжении. Правила сертификации питьевой воды, расфасованной в емкости» (М.: Госстандарт, 1995).
25. ГОСТ Р «Вода питьевая, расфасованная в емкости. Общие технические условия» (Проект. М.: Госстандарт, 1999).
26. Proposed Draft General Standard for Packaged (Bottled) Waters others then Natural Waters (ALINORM 9920, Appendix II).
27. The Codex General Standard for Food Additions (CODEX-STAN 192-1995, Rev. 1 - 1997).
28. The Recommended International Code of Practice - General Principles of Food Hygiene (CAC/ RCP1-1969, Rev. 3 - 1997).
29. The Codex of Hygiene Practice for Packaged (Bottled) Drinking Waters (other than Natural Mineral Water) - Draft (Being developed by the Codex Committee on Food Hygiene).
30. The Principles for the Establishment and Application of Microbiological Criteria for Foods (CACGL 21 - 1997).
31. The Codex General Standard for the Labelling of Prepackaged Foods (CODEX STAN1-1885, Rev. 1 - 1991).
32. The Standard for Natural Mineral Waters (CODEX STAN 108-1981, Rev. 1 - 1997).
33. Guidelines on Health Aspects of Water Desalination. Who, Geneva, ETS/80.4, 1980. - 60 p.
34. Plant Technical Manual. IBWA. Revised, 1987. - 285 p.
Приложение 1
(справочное)
Классификация расфасованных вод по общему солесодержанию, видам получения и использования
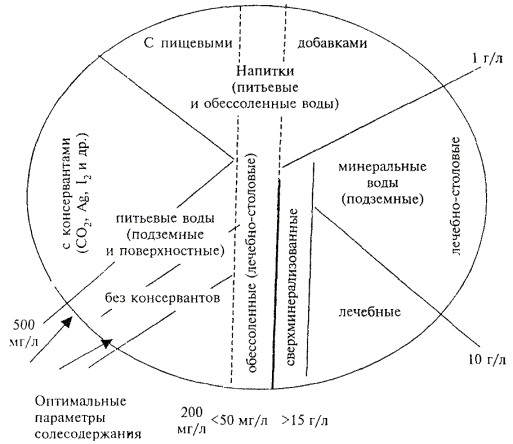
|
Питьевые (пресные) воды: |
Минеральные воды (солоноватые, соленые, рассолы): |
Обессоленные (ультрапресные) воды: |
|
• нативные (природные) • скорректированные по хим. составу, органолептическим и физическим свойствам • полученные искусственным путем |
• нативные (природные) • скорректированные по хим. составу и органолептическим свойствам |
• нативные • полученные искусственным путем |
Расфасованные питьевые воды должны обеспечить население не только питьевой водой, полностью отвечающей санитарным правилам и нормам, но и водой, специально предназначенной для сохранения и укрепления здоровья, что особенно важно для наиболее уязвимых, «критических» групп населения. Вода, содержащая оптимальные уровни биологически необходимых макроэлементов (кальция, магния, фосфатов) и некоторых микроэлементов (селен, калий, цинк, йод, фтор и др.), полезна и необходима детям, особенно в раннем возрасте, беременным, а также лицам пожилого возраста. Лица, страдающие хроническими заболеваниями печени и почек, нуждаются в воде, не только скорректированной по солевому составу, но и практически не содержащей токсичные вещества. Детям с гипертензивным синдромом, согласно рекомендациям ВОЗ, показано не только регламентированное потребление соли, но и ограничение содержания натрия и хлоридов в питьевой воде. Огромную проблему для 85 % населения России представляют йодо- и фтородефициты и связанная с ними эндокрино- и стоматологическая патология. Почти повсеместно отмечено нарастание дефицита поступления в организм как детского, так и взрослого населения солей кальция и других биогенных элементов.
Приложение 2
(обязательное)
Форма протокола испытаний образцов исходной («сырьевой») питьевой воды для промышленного розлива
Полное наименование испытательного центра (лаборатории) № аттестата аккредитации в системе ЦГСЭН МЗ РФ, адрес, телефон/факс
ПРОТОКОЛ №
от «день, месяц, год»
|
Результаты физико-химического, микробиологического, паразитологического, радиологического и экспресс-токсикологического анализа пробы виды («сырьевой») 1. Наименование предприятия, организации (заявитель) ______________________________________________________________ 2. Юридический адрес ____________________________________________________ 3. Место взятия пробы _____________________________________________________ (место нахождения водоисточника, № скважины) _____________________________ 4. Наименование пробы ___________________________________________________ 5. Дополнительные сведения (для подземных источников: водоносный горизонт, интервал опробования; для водопроводных вод из поверхностных источников: технология водоподготовки) _______________________________________________ 6. Условия отбора ________________________________________________________ 7. Дата и время отбора ____________________________________________________ 8. Кем отобрана проба _____________________________________________________ 9. Условия доставки ______________________________________________________ 10. Специфические вещества, характерные для местных условий _________________ |
Таблица
|
№ п.п. |
Показатели |
Единицы измерения |
Результаты анализа пробы воды |
Метод анализа |
|
1 |
2 |
3 |
4 |
5 |
|
I. Органолептические показатели |
||||
|
1 |
Запах |
баллы |
|
|
|
2 |
Привкус |
» |
|
|
|
3 |
Цветность |
град. |
|
|
|
4 |
Мутность |
ЕМФ (единицы мутности по формазину) |
|
|
|
5 |
Водородный показатель |
рН |
|
|
|
II. Солевой и газовый состав |
||||
|
6 |
Общая минерализация |
мг/л |
|
|
|
7 |
Сухой остаток |
» |
|
|
|
8 |
Щелочность |
мг-экв/л |
|
|
|
9 |
Жесткость |
мг-экв/л |
|
|
|
10 |
Кальций (Са) |
мг/л |
|
|
|
11 |
Магний (Mg) |
» |
|
|
|
12 |
Калий (К) |
» |
|
|
|
13 |
Натрий (Na) |
» |
|
|
|
14 |
Бикарбонаты (НСО3) |
» |
|
|
|
15 |
Фторид-ион (F) |
» |
|
|
|
16 |
Хлориды (Сl-) |
» |
|
|
|
17 |
Сульфаты (SO4-) |
» |
|
|
|
18 |
Фосфаты (РО4) |
» |
|
|
|
19 |
Силикаты (по Si) |
» |
|
|
|
20 |
Нитраты (по NO3) |
» |
|
|
|
21 |
Цианиды (по CN-) |
» |
|
|
|
22 |
Кислород (О2) |
» |
|
|
|
23 |
Углекислота свободная (СO2) |
» |
|
|
|
24 |
Сероводород (H2S) |
» |
|
|
|
III. Показатели органического загрязнения |
||||
|
25 |
Окисляемость перманганатная |
мг О2/л |
|
|
|
26 |
Нитриты (по NO2) |
мг/л |
|
|
|
27 |
Аммиак и аммоний-ион (NH4) |
» |
|
|
|
28 |
Общий углерод |
» |
|
|
|
29 |
Органический углерод |
» |
|
|
|
30 |
Неорганический углерод |
» |
|
|
|
31 |
ПАВ (анионоактивные) |
» |
|
|
|
32 |
Нефтепродукты |
» |
|
|
|
33 |
Фенолы летучие, суммарно |
мкг/л |
|
|
|
34 |
Хлороформ |
» |
|
|
|
35 |
Бромоформ* |
» |
|
|
|
36 |
Дибромхлорметан* |
» |
|
|
|
37 |
Бромдихлорметан* |
» |
|
|
|
38 |
1,2-дихлорэтан** |
» |
|
|
|
39 |
1,2-дихлорэтилен** |
» |
|
|
|
40 |
Тетрахлорэтилен** |
» |
|
|
|
41 |
Трихлорэтилен** |
» |
|
|
|
42 |
Дихлорметан** |
» |
|
|
|
43 |
Четыреххлористый углерод |
» |
|
|
|
44 |
Формальдегид |
» |
|
|
|
45 |
Бенз(а)пирен |
» |
|
|
|
46 |
Ди(2-этилгексил)фталат |
» |
|
|
|
47 |
Гексахлорбензол |
» |
|
|
|
48 |
Линдан (гамма- изомер ГХЦГ) |
» |
|
|
|
49 |
2,4-Д |
» |
|
|
|
50 |
Гептахлор |
» |
|
|
|
51 |
ДДТ (сумма изомеров) |
» |
|
|
|
52 |
Атразин |
» |
|
|
|
53 |
Симазин |
» |
|
|
|
IV. Металлы |
||||
|
54 |
Алюминий (Аl) |
мг/л |
|
|
|
55 |
Барий (Ва) |
» |
|
|
|
56 |
Берилий (Be) |
» |
|
|
|
57 |
Железо (Fe, суммарно) |
» |
|
|
|
58 |
Кадмий (Cd, суммарно) |
» |
|
|
|
59 |
Кобальт (Со) |
» |
|
|
|
60 |
Литий (Li) |
» |
|
|
|
61 |
Марганец (Mn) |
» |
|
|
|
62 |
Медь (Cu, суммарно) |
» |
|
|
|
63 |
Молибден (Mo, суммарно) |
» |
|
|
|
64 |
Никель (Ni, суммарно) |
» |
|
|
|
65 |
Ртуть (Hg, суммарно) |
» |
|
|
|
66 |
Селен (Se) |
» |
|
|
|
67 |
Серебро (Ag) |
» |
|
|
|
68 |
Свинец (Рb, суммарно) |
» |
|
|
|
69 |
Стронций (Sr2+) |
» |
|
|
|
70 |
Сурьма (Sb) |
» |
|
|
|
71 |
Хром (Сr6+) |
» |
|
|
|
72 |
Цинк (Zn2+) |
» |
|
|
|
V. Галогены |
||||
|
73 |
Бромид-ион |
мг/л |
|
|
|
74 |
Хлор остаточный свободный |
» |
|
|
|
75 |
Хлор остаточный связанный |
» |
|
|
|
76 |
Озон |
» |
|
|
|
77 |
Йодид-ион |
» |
|
|
|
VI. Неметаллические элементы |
||||
|
78 |
Бор (В) |
мг/л |
|
|
|
79 |
Мышьяк (As) |
» |
|
|
|
VII. Микробиологические, показатели |
||||
|
80 |
Глюкозоположительные колиформные бактерии*** |
КОЕ/100 мл |
|
|
|
81 |
Общие колиформные бактерии |
КОЕ/100 мл |
|
|
|
82 |
Термотолерантные колиформные бактерии |
КОЕ/100 мл |
|
|
|
83 |
ОМЧ при температуре 37 °С |
КОЕ/мл |
|
|
|
84 |
ОМЧ при температуре 22 °С |
КОЕ/мл |
|
|
|
85 |
E. coli |
КОЕ/100 мл |
|
|
|
86 |
Споры сульфитредуцирующих клостридий**** |
КОЕ/100 мл |
|
|
|
87 |
Энтерококки |
КОЕ/100 мл |
|
|
|
88 |
Колифаги |
КОЕ/100 мл |
|
|
|
89 |
Патогенные бактерии кишечной группы |
1000 мл |
|
|
|
90 |
Энтеровирусы |
10 л |
|
|
|
VIII. Паразитологические показатели*** |
||||
|
91 |
Ооцисты криптоспоридий |
Кол-во в 50 л |
|
|
|
92 |
Цисты лямблий |
Кол-во в 50 л |
|
|
|
93 |
Яйца гельминтов |
Кол-во в 50 л |
|
|
|
IX. Показатели радиоактивного загрязнения |
||||
|
94 |
Удельная суммарная a - радиоактивность |
Бк/л |
|
|
|
95 |
Удельная суммарная b - риадиоактивность |
» |
|
|
|
X. Биотестирование |
||||
|
96 |
Дафнии (время выживаемости) |
часы |
|
|
|
97 |
Инфузории |
К токc. |
|
|
|
98 |
Эколюм (бактерии) |
Степень изменения свечения, % |
|
|
|
99 |
Тест Эймса на Salmonella thyphimurium (суммарная мутагенная активность) |
Уровень суммарной мутагенной активности |
|
|
|
XI. Коррозионная активность |
||||
|
100 |
П1 |
Единицы |
|
|
|
101 |
П2 |
Единицы |
|
|
|
XII. Комплексные показатели |
||||
|
102 |
По S NO2и NO3 |
Единицы |
|
|
|
103 |
По S тригалометанов |
» |
|
|
|
104 |
По S ХОС |
» |
|
|
|
Примечания: 1. * - анализ выполняется только в пробах питьевой воды из централизованных систем питьевого водоснабжения. ** - указанные показатели являются рекомендуемыми до внесения изменений в СанПиН 2.1.4.1074-01. *** - анализ выполняется только в пробах воды подземных водоисточников. **** - анализ выполняется только в пробах воды поверхностных источников питьевой воды из централизованных систем питьевого водоснабжения из поверхностных источников. 2. В случае невозможности выполнения полного анализа на базе испытательного центра исследования по отдельным разделам выполняются в других аккредитованных на данный вид исследований лабораториях (центрах). При этом форма протокола аналогична представленной. |
||||
Ф. И. О., должность специалистов, проводивших исследования:
Дата выполнения анализа «____»__________ г.
Заключение
Руководитель испытательной
лаборатории (Ф. И. О.)
Приложение 3
(обязательное)
Форма протокола испытаний питьевых вод, расфасованных в емкости
Полное наименование испытательного центра (лаборатории), № аттестата аккредитации в системе ЦГСЭН МЗ РФ или в системе ГОСТ Р, адрес, телефон/факс
ПРОТОКОЛ №
от «день, месяц, год»
Результаты физико-химического, микробиологического и экспресс-токсикологического анализа пробы расфасованной воды, при хранении в различных температурных условиях
|
Наименование предприятия, организации (заявитель) __________________________ Юридический адрес ______________________________________________________ Наименование продукции _________________________________________________ Дата розлива _____________________________________________________________ Дата и время отбора ______________________________________________________ Кем отобрана проба _______________________________________________________ Условия доставки ________________________________________________________ |
Таблица
|
№ п.п. |
Показатели |
Единицы измерения |
Результат анализа пробы воды при температуре хранения, °С |
Метод анализа |
||
|
+4 |
+22 |
+37 |
||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
I. Органолептические показатели |
||||||
|
1 |
Запах |
баллы |
|
|
|
|
|
2 |
Привкус |
» |
|
|
|
|
|
3 |
Цветность |
град. |
|
|
|
|
|
4 |
Мутность |
ЕМФ (единицы мутности по формазину) |
|
|
|
|
|
5 |
Водородный показатель |
рH |
|
|
|
|
|
II. Солевой и газовый состав |
||||||
|
6 |
Щелочность |
Мг-экв/л |
|
|
|
|
|
7 |
Жесткость |
Мг-экв/л |
|
|
|
|
|
8 |
Кальций (Ca) |
мг/л |
|
|
|
|
|
9 |
Магний (Mg) |
» |
|
|
|
|
|
10 |
Бикарбонаты (HCO3) |
» |
|
|
|
|
|
11 |
Фторид-ион (F) |
» |
|
|
|
|
|
12 |
Сульфаты (SO4_) |
» |
|
|
|
|
|
13 |
Нитраты (по NO3) |
» |
|
|
|
|
|
14 |
Кислород (О2) |
» |
|
|
|
|
|
15 |
Углекислота свободная (СO2) |
» |
|
|
|
|
|
16 |
Сероводород (H2S) |
» |
|
|
|
|
|
III. Показатели органического загрязнения |
||||||
|
17 |
Окисляемость перманганатная |
мг О2/л |
|
|
|
|
|
18 |
Нитраты (по NO2) |
мг/л |
|
|
|
|
|
19 |
Аммиак и аммоний-ион (NH4) |
» |
|
|
|
|
|
20 |
Общий углерод |
» |
|
|
|
|
|
21 |
Органический углерод |
» |
|
|
|
|
|
22 |
Неорганический углерод |
мг/л |
|
|
|
|
|
23 |
Фенолы летучие, суммарно |
мкг/л |
|
|
|
|
|
24 |
Хлороформ* |
» |
|
|
|
|
|
25 |
Бромоформ* |
» |
|
|
|
|
|
26 |
Четыреххлористый углерод* |
» |
|
|
|
|
|
27 |
Формальдегид** |
» |
|
|
|
|
|
28 |
Ди(2-этилгексил)-фталат |
» |
|
|
|
|
|
29 |
Продукты миграции токсичных веществ из тары в зависимости от материала тары |
мг/л |
в соответствии с табл. 1.4. |
|
|
|
|
IV. Металлы |
||||||
|
30 |
Алюминий (Аl) |
мг/л |
|
|
|
|
|
31 |
Железо (Fe, суммарно) |
» |
|
|
|
|
|
32 |
Серебро (Ag) |
» |
|
|
|
|
|
33 |
Цинк (Zn) |
» |
|
|
|
|
|
V. Галогены |
||||||
|
34 |
Бромид ион |
мг/л |
|
|
|
|
|
35 |
Хлор остаточный связанный* |
» |
|
|
|
|
|
36 |
Йодид ион |
» |
|
|
|
|
|
VI. Неметаллические элементы |
||||||
|
37 |
Бор (В) |
мг/л |
|
|
|
|
|
VII. Микробиологические показатели |
||||||
|
38 |
ОМЧ при 22 °С 37 °С |
КОЕ/мл |
|
|
|
|
|
39 |
Общие колиформные бактерии |
КОЕ/100 мл |
|
|
|
|
|
40 |
Термотолерантные колиформные бактерии |
КОЕ/100 мл |
|
|
|
|
|
41 |
Глюкозоположительные колиформные бактерии |
КОЕ/100 мл |
|
|
|
|
|
42 |
Споры сульфитредуцирующих клостридий*** |
КОЕ/100 мл |
|
|
|
|
|
43 |
Pseudomonas aemginosa |
Обнаружение в 1000 мл |
|
|
|
|
|
44 |
Колифаги |
БОЕ/1000 мл |
|
|
|
|
|
Примечания: 1. * - анализ выполняется только в расфасованной воде, источником которой является питьевая вода из централизованных систем питьевого водоснабжения. ** - анализ выполняется только после изменения технологии водоподготовки. *** - анализ выполняется только в расфасованной воде, источником которой служит вода поверхностных водоемов или централизованных систем питьевого водоснабжения с водозабором из поверхностных источников. 2. В случае невозможности выполнения полного анализа на базе испытательного центра исследования по отдельным разделам выполняются в других аккредитованных на данный вид исследований лабораториях (центрах). При этом форма протокола аналогична представленной. 3. В случае отсутствия результатов углубленного анализа исходной («сырьевой») воды исследование расфасованной питьевой воды при t 20 - 22 °С проводится в полном объеме по показателям, представленным в таблице приложения 4. |
||||||
Ф. И. О., должность специалистов, проводивших исследования:
Дата выполнения анализа «___»____________ г.
Заключение.
Руководитель испытательной
лаборатории (Ф. И. О.)
Приложение 4
Необходимые объемы воды для различных видов анализа при гигиенической оценке питьевой воды, подлежащей бутылированию
|
Вид анализа |
Объем пробы, дм3 |
Примечания |
|
Физико-химический: |
|
|
|
- органолептические свойства; |
0,5 |
Без консервации |
|
- солевой состав; |
1 |
Без консервации |
|
- металлы; |
0,5 |
Подкисление до рН менее 2 |
|
- микроэлементы (бор, бром, фтор, йод); |
2 |
Без консервации |
|
- газовый состав: |
|
|
|
- кислород (О2) |
0,3 |
Без консервации |
|
- углекислота свободная (СO2) |
0,5 |
Без консервации |
|
- сероводород (H2S) |
0,3 |
Без консервации |
|
- органический углерод, перманганатная окисляемость; |
1 |
Подкисление до рН менее 2 серной кислотой |
|
- бенз(а)пирен; |
3 |
Консервация растворителем, используемым для экстракции |
|
- ПАВы |
0,1 |
Консервация хлороформом 0,2 - 0,4 см3 |
|
- нефтепродукты; |
1 |
Подкисление до рН менее 2 |
|
- пестициды; |
1 |
Консервация растворителем, используемым для экстракции |
|
- фенолы; |
1 |
Консервация 4 г NaOH |
|
- остаточные дозы дезинфектантов; |
0,5 |
Без консервации |
|
- содержание летучих хлорсодержащих соединений и других органических веществ по данным хроматомасс-спектрометрии |
0,3 |
Без консервации, охлаждение до 2 - 5 °С |
|
Радиологический |
3 - 5 |
Консервация азотной кислотой до рН менее 1 |
|
Биотестирование: |
|
|
|
- суммарная мутагенная активность; |
200 |
Концентрация на фильтрах с сепароном |
|
- гидробионты |
0,5 |
Стерильные условия |
|
Бактериологический |
3 |
Стерильные условия |
|
Вирусологический |
10 |
Стерильные условия |
|
Паразитологический |
25 (источник) или 50 (водопроводная вода) |
Концентрация на мембранном фильтре № 3 |
Приложение 5
(обязательное)
Перечень показателей качества расфасованной воды и методики их контроля для полного анализа
|
Показатели |
Единицы измерения |
Нормативные документы, определяющие методы контроля |
Чувствительность метода |
|
1 |
2 |
3 |
4 |
|
1. Органолептические показатели |
|||
|
1.1. Запах |
Баллы |
ГОСТ 3351-74; РД 52.24.496-95 |
- |
|
1.2. Привкус |
Баллы |
ГОСТ 3351-74 |
- |
|
1.3. Цветность |
град. |
ГОСТ 3351-74; РД 52.24.497-95 |
5 |
|
1.4. Мутность |
ЕМФ (единицы мутности по формазину) |
ГОСТ 3351-74 |
0,1 |
|
1.5. Водородный показатель |
Единицы РН |
РД 52.24.495-95 |
4 |
|
2. Солевой и газовый состав |
|||
|
2.1. Общая минерализация (сухой остаток) |
мг/л |
ГОСТ 18164-82 |
- |
|
2.2. Щелочность |
ммоль/л |
ИСО 9963-1-86 |
0,4 |
|
2.3. Жесткость |
мг-экв/л |
РД 52.24.395-95; |
0,5 |
|
2.4. Кальций (Ca) |
мг/л |
ИСО 11885-96; ГОСТ Р 51309-99 |
0,01 |
|
2.5. Магний (Mg) |
» |
» |
0,05 |
|
2.6. Калий (К) |
мг/л |
ИСО 9964-3-96; ГОСТ Р 51309-99 |
0,1 |
|
2.7. Натрий (Na) |
» |
ГОСТ Р 51309-99 |
0,1 |
|
2.8. Бикарбонаты (HCO3) |
» |
РД 52.24.493-95 |
10 |
|
2.9. Фторид-ион (F) |
» |
ГОСТ 4386-89 |
0,1 |
|
2.10. Хлориды (Сl-) |
» |
ГОСТ 4245-98 |
0,5 |
|
2.11. Сульфаты (SO4-) |
» |
ГОСТ 4389-98 |
2 |
|
2.12. Фосфаты (РO4-) |
» |
ГОСТ 18309-98 |
0,01 |
|
2.13. Силикаты (по SiO2) |
» |
УМИКВ. Ч. 1 М. СЭВ, 1987 |
0,01 |
|
2.14. Нитраты (по NO3-) |
» |
РД 52.24.380-95; |
0,1 |
|
2.15. Цианиды (по CN-) |
» |
ИСО 6703 П 57/98 |
0,01 |
|
2.16. Кислород (О2) |
» |
РД 52.24.419-95 |
1 |
|
2.17. Озон (О3) |
» |
ГОСТ 1830-72 |
0,05 |
|
2.18. Углекислота свободная (CO2) |
» |
УМИКВ. Ч. 1. М. СЭВ, 1987 |
1 |
|
2.19. Сероводород (H2S) |
» |
ИСО 10530, РД 52.24.450-95 |
2 |
|
3. Показатели органического загрязнения |
|||
|
3.1. Окисляемость перманганатная |
мг О2/л |
ИСО 8467-93. Определение перманганатного индекса |
0,5 |
|
3.2. Нитриты (по NO2-) |
мг/л |
ИСО 10304-1-92; ИСО 6777-84; МУК 4.1.065-96; ГОСТ 4192-82 |
0,003 |
|
3.3. Аммиак и аммоний-ион (NH4) |
» |
ГОСТ 4192-98 |
0,05 |
|
3.4. Органический углерод |
» |
ИСО 8245-93 |
0,3 |
|
3.5. ПАВ (анионоактивные) |
» |
РД 52.24.27-86; ИСО 7875/1,2-84; ГОСТ Р 51211-98 |
0,01 |
|
3.6. Нефтепродукты |
» |
РД 52.24.453-95; РД 52.24.476-95; МУК 4.1.068-96 |
0,05 0,05 0,04 0,005 |
|
3.7. Фенолы летучие, суммарно |
мкг/л |
РД 52.24.480-95; РД 52.24.487-95; МУК 4.1.069-96 |
2 0,5 0,5 |
|
3.8. Хлороформ |
мг/л |
ГОСТ Р 51392-99; РД 52.24.482-95; МУК 4.1.646-96 |
0,0015 |
|
3.9. Бромоформ |
» |
ГОСТ Р 51392-99; МУК 4.1.646-96 |
0,0006 |
|
3.10. Дибромхлорметан |
» |
» |
0,0003 |
|
3.11. Бромдихлорметан |
» |
» |
0,0003 |
|
3.12. 1,2-дихлорэтан* |
» |
» |
0,005 |
|
3.13. 1,1-дихлорэтилен* |
» |
» |
0,012 |
|
3.14. Тетрахлорэтилен* |
мг/л |
ГОСТ Р 51392-99; МУК 4.1.646-96 |
0,0001 |
|
3.15. Трихлорэтилен* |
» |
» |
0,0001 |
|
3.16. Дихлорметан* |
|
» |
0,0003 |
|
3.17. Четыреххлорисгый углерод |
» |
» |
0,0001 |
|
3.18. Формальдегид |
» |
РД 52.24.492-95; ПНДФ 14.1:1:4.120-96 |
0,025 |
|
3.19. Бенз(а)пирен |
мкг/л |
ГОСТ Р 51310-99; А-7/12-94 |
0,002 |
|
3.20. Ди(2-этилгексил) фталат |
Мг/л |
МУК 4.1.738-99 |
0,1 |
|
3.21. Гексахлорбензол |
мкг/л |
МУ М3 № 4120-86 |
0,1 |
|
3.22. Линдан (гамма-изомер ГХЦГ) |
» |
ГОСТ Р 51209-98 |
0,1 |
|
3.23. 2,4-Д |
» |
РД 52.24.438-95 |
0,05 |
|
3.24. Гептахлор |
» |
ГОСТ Р 51209-98 |
0,02 |
|
3.25. ДДТ (сумма изомеров) |
» |
ГОСТ Р 5120-98 |
0,1 |
|
3.26 Атразин |
» |
РД 52.24.40-95; А-5/12-94 |
1 0,5 |
|
3.27. Симазин |
» |
РД 52.24.410-95; А-5/12-94 |
1 0,5 |
|
4. Металлы |
|||
|
4.1. Алюминий (Аl) |
мг/л |
ГОСТ Р 51309-99; РД 52.24.377-95; ИСО 11885-96; МУК 4.1.057-96; ГОСТ 18165-81 |
0,01 |
|
4.2. Барий (Ba) |
» |
ГОСТ Р 51309-99 Унифицированные методы исследования качества вод СЭВ. Ч. 1. Т. 2 М, 1987; ИСО 11885-96 |
0,01 |
|
4.3. Берилий (Be) |
» |
ГОСТ Р 51309-99; ИСО 11885-96 |
0,0001 |
|
4.4. Железо (Fe, суммарно) |
» |
ГОСТ Р 51309-99 |
0,1 0,04 |
|
4.5. Кадмий (Cd, суммарно) |
» |
ГОСТ Р 51309-99; РД 52.24.436-95; ИСО 11885-96, ИСО 8288-86; ИСО 5961-94 |
0,0001 |
|
4.6. Кобальт (Co) |
» |
ГОСТ Р 51309-99; ИСО 11885-96 |
0,001 |
|
4.7. Литий (Li) |
» |
» |
0,001 |
|
4.8. Марганец (Mn) |
» |
ГОСТ Р 51309-99; ГОСТ 4974-72 |
0,001 |
|
4.9. Медь (Cu, суммарно) |
» |
ГОСТ Р 51309-99; ГОСТ 4388-72 |
0,01 |
|
4.10. Молибден (Mo, суммарно) |
» |
ГОСТ Р 51309-99; ИСО 11885-96; РД 52.24.377-95; РД 33-5.302-96; ГОСТ 8308-72 |
0,001 |
|
4.11. Никель (Ni, суммарно) |
» |
ГОСТ Р 51309-99; РД 52.24.377-95; ИСО 118856-96; РД 52.24.494-95 |
0,001 |
|
4.12. Ртуть (Hg, суммарно) |
мкг/л |
ГОСТ Р 51212-98; РД 52.24.479-95 |
0,1 0,02 |
|
4.13. Селен (Se) |
» |
ГОСТ Р 51309-99; ИСО 9965; ИСО 11885-96 |
0,002 |
|
4.14. Серебро (Ag) |
» |
ГОСТ Р 51309-99; ИСО 11885-96; ГОСТ 51309-99 |
0,0005 |
|
4.15. Свинец (Pb, суммарно) |
» |
ГОСТ Р 51309-99; ИСО 11885-96; РД 52.24.377-95; РД 52.24.371-95; ГОСТ 18293-72 |
0,001 |
|
4.16. Стронций (Sr) |
» |
ГОСТ Р 51309-99; ГОСТ 23950-88; ИСО 11885-96 |
0,001 |
|
4.17. Сурьма (Sb) |
» |
ГОСТ Р 51309-99; ИСО 11885-96 |
0,005 |
|
4.18. Хром (Cr6+) |
» |
ГОСТ Р 51309-99; ИСО 11885-96; РД 52.24.377-95; РД 52.24.446-95; ИСО 9174-90 |
0,001 |
|
4.19. Цинк (Zn) |
» |
ГОСТ Р 51309-99; ГОСТ 18293-72 |
0,001 |
|
5. Галогены |
|||
|
5.1. Бромид-ион |
мг/л |
Унифицированные методы исследования качества вод. СЭВ. Ч. 1. T. 2. M., 1987 |
0,1 |
|
5.2. Хлор остаточный свободный |
» |
ГОСТ 18190-72 |
0,01 |
|
5.3. Хлор остаточный связанный |
» |
» |
0,01 |
|
5.4. Озон |
» |
ГОСТ 1830-72 |
0,05 |
|
5.5. Йодид-ион |
» |
МУК 4.1.1106-02 Унифицированные методы исследования качества вод. СЭВ. Ч. 1. Т. 2. М., 1987 |
0,01 |
|
6. Неметаллические элементы |
|||
|
6.1. Бор (В) |
мг/л |
ГОСТ 51210-98 |
0,05 |
|
6.2. Мышьяк (As) |
» |
ГОСТ 5 1309-99; ИСО 11885-96 |
0,005 |
|
7. Микробиологические показатели |
|||
|
7.1. ОМЧ при температуре 37 °С |
КОЕ/мл |
Методические указания. Санитарно-микробиологический анализ питьевой воды. МУ 4.2.1018-01 |
|
|
7.2. ОМЧ при температуре 22 °С |
КОЕ/мл |
Приложение 11 настоящих МУ |
|
|
7.3. Общие колиформные бактерии |
КОЕ/100 мл |
Методические указания. Санитарно-микробиологический анализ питьевой воды. МУ 4.2.1018-01 Приложение 9 настоящих МУ |
|
|
7.4. Глюкозоположительные колиформные бактерии |
» |
Приложение 9 настоящих МУ |
|
|
7.5. Термотолерантные колиформные бактерии |
» |
Методические указания. Санитарно-микробиологический анализ питьевой воды. МУ 4.2.1018-01 |
|
|
7.6. Споры сульфитредуцирующих клостридий |
КОЕ/100 мл |
Методические указания. Санитарно- микробиологический анализ питьевой воды. МУ 4.2.1018-01 |
|
|
7.7. Pseudomonas aeruginosa |
Обнаружение в 1000 мл |
Методические рекомендации по обнаружению и идентификации Pseudomonas aeruginosa в объектах окружающей среды (пищевых продуктах, воде, сточных жидкостях). М., 1984. Приложение 10 настоящих МУ |
|
|
7.8. Патогенные бактерии кишечной группы (сальмонеллы, шигеллы) |
» |
Методические указания по санитарно-микробиологическому анализу водных поверхностных водоемов № 2285-81 |
|
|
7.9. Колифаги |
БОЕ/1000 мл |
Методические указания. Санитарно-микробиологический анализ питьевой воды. МУ 4.2.1018-01 Приложение 12 настоящих МУ |
|
|
7.10. Энтеровирусы |
Обнаружение в 10 л |
Методические рекомендации по организации и проведению эпидемиологического и санитарно-вирусологического надзора за качеством воды водоисточников, питьевой воды в системе водоснабжения с целью профилактики заболеваемости гепатитом А и др. кишечными вирусными инфекциями. МР 01-19/12-13 от 11.09.92 МЗ РФ |
|
|
8. Паразитологические показатели |
|||
|
8.1. Ооцисты криптоспоридий |
Кол-во в 50 л |
ISO TC147/SC 4 № 0204 «Isolation and identification of Cryptosporidium Oocysts and Giardia Cysts from water» (2002-01-22) |
|
|
8.2. Цисты лямблий |
Кол-во в 50 л |
Санитарно-паразитологические исследования воды хозяйственного и питьевого использования. МУК 4.2.964-00 |
|
|
8.3. Яйца гельминтов |
Кол-во в 50 л |
» |
|
|
9. Показатели радиоактивного загрязнения |
|||
|
9.1. Суммарная a - радиоактивность |
Бк/л |
ИСО 9696-92 |
0,1 |
|
9.2. Суммарная b - радиоактивность |
» |
ИСО 9697-92 |
0,5 |
|
X. Биотестирование |
|||
|
10.1. Дафнии (время выживаемости) |
Часы |
MPNЦОС ПВР 005-95; Методические рекомендации по применению методов биотестирования для оценки качества воды в системе хозяйственно-питьевого водоснабжения |
|
|
10.2. Инфузории |
К токc. |
» |
|
|
10.3. Эколюм (бактерии) |
Степень изменения свечения, % |
» |
|
|
10.4. Тест Эймса на Salmonella thyphimurium (суммарная мутагенная активность) |
Уровень суммарной мутагенной активности |
Методические указания по экспериментальной оценке суммарной мутагенной активности воздуха и воды. М., 1990 |
|
|
XI. Комплексные показатели* |
|||
|
11.1. По S NO2 и NO3 |
Единицы |
Расчетно |
|
|
11.2. По S токсичных металлов (I и II класс опасности) |
Единицы |
Расчетно |
|
|
11.3. По S тригалометанов |
» |
Расчетно |
|
|
Примечание. * - Рассчитываются по формуле:
где Q1 - содержание в воде конкретного в-ва в мг/(мкг)/л; ПДК - предельно допустимая концентрация этого вещества в воде в мг (мкг)/л; Рекомендуемая величина S £ 1. |
|||
Приложение 6
Оценочные показатели миграции химических веществ в расфасованную воду из полимерных материалов упаковки и стеклянной тары
|
Показатели |
ПДК, мг/л, не более |
Класс опасности |
Материалы |
|||
|
Полиэтилен |
ПЭТ |
Поликарбонат |
Стекло |
|||
|
Бутанол |
0,2 |
2 |
|
|
+ |
|
|
Винилхлорид |
0,05 |
2 |
|
|
|
|
|
Гексан |
0,01 |
2 |
|
|
+ |
|
|
Гептан |
0,005 |
2 |
|
|
+ |
|
|
Метанол |
3 |
2 |
|
|
+ |
|
|
Формальдегид |
0,05 |
2 |
+ |
+ |
+ |
|
|
Этилацетат |
0,2 |
2 |
+ |
+ |
|
|
|
Фталаты (пластификаторы) |
0,5 |
3 |
+ |
+ |
|
|
|
Изопропанол |
0,25 |
4 |
+ |
+ |
|
|
|
Ацетон |
2,2 |
3 |
+ |
+ |
|
|
|
Толуол |
0,5 |
4 |
+ |
+ |
+ |
|
|
Бензол |
0,5 |
2 |
+ |
+ |
+ |
|
|
Ксилол |
0,05 |
3 |
+ |
+ |
+ |
|
|
Бор |
0,5 |
|
|
|
|
+ |
Приложение 7
(обязательное)
Метод определения общего числа микроорганизмов, образующих колонии на питательном агаре (ОМЧ)
Оборудование, расходные материалы, питательные среды, метод посева и учет результатов - в соответствии с МУК 4.2.1018-01 «Санитарно-микробиологический анализ питьевой воды».
При определении показателя ОМЧ при 37 °С делают посев по 1 мл в две чашки Петри. При необходимости определения двух показателей ОМЧ при 37 °С и при 22 °С посев по 1 мл производят в четыре чашки Петри (по две чашки Петри на каждую температуру). Посевы производят при горящей спиртовке.
Приоткрыв крышку чашки Петри, посев заливают небольшим количеством (8 - 10 мл) питательного агара, охлажденного до температуры 45 - 46 °С. Заливку питательного агара производят после фламбирования краев емкости. Посев немедленно смешивают с питательным агаром, плавными вращательными движениями, избегая попадания на края и крышку чашки Петри, и оставляют на ровной горизонтальной поверхности. Время между внесением пробы и агара не должно превышать 10 - 15 минут.
После полного застывания чашки переворачивают крышкой вниз и две инкубируют при температуре (37 ± 1) °С в течение (24 ± 2) часа, и две - инкубируют при температуре (22 ± 1)°С в течение (68 ± 4) часа.
При учете результатов подсчитывают все колонии на двух параллельных чашках, видимые при увеличении в два раза, и вычисляют среднее арифметическое. Результат выражают числом колоний в 1 мл пробы воды и выдают ответ - число КОЕ ОМЧ в 1 мл при 37 °С и при 22 °С.
Приложение 8
(обязательное)
Ускоренный метод определения общих и глюкозоположительных колиформных бактерий
Обнаружение ОКБ в расфасованной воде выполняют методом мембранной фильтрации или титрационным по МУК 4.2.1018-01.
При необходимости получения быстрого ответа о качестве воды, при производственном контроле определение ОКБ и ГКБ проводят ускоренным методом.
Определение общих колиформных бактерий методом мембранной фильтрации
Принцип метода заключается в использовании на этапе идентификации комбинации двух признаков ОКБ: первый (основной) - характер роста колоний на лактозной среде Эндо - темно-красные с отпечатком на обратной стороне фильтра, что подтверждает способность ферментировать лактозу до кислоты; второй - отрицательный оксидазный тест или способность к газообразованию. Поскольку лактозоположительные бактерии, ферментирующие лактозу до кислоты и газа, аналогично ферментируют глюкозу, то газообразование можно подтвердить на средах с любым углеводом, однако, использование подтверждающих сред с глюкозой целесообразнее, т. к. сокращает время анализа на сутки.
Выполнение анализа
Подготовка посуды, питательных сред и реактивов, техника мембранной фильтрации выполняется по МУК 4.2.1018-01.
Объем пробы воды 300 мл профильтровывают через мембранные фильтры, помещают на среду Эндо. Чашки с посевами ставят в термостат дном вверх и инкубируют при температуре (37 ± 1) °С в течение 24 ± 2 часа.
Если после инкубации на фильтрах нет роста или выросли колонии, не характерные для колиформных бактерий - плесневые, морщинистые, пленчатые, губчатые, расплывчатые, прозрачные - выдают отрицательный ответ.
Если на фильтрах обнаружен рост типичных для лактозоположительных бактерий колоний (выявляются благодаря дифференциальным свойствам лактозной среды Эндо) - темно-красных, красных с металлическим блеском или без него, слизистых розовых с отпечатком на обратной стороне фильтра - следует подтвердить их принадлежность к ОКБ. Для этой цели можно использовать один из вариантов.
Первый вариант
Выполняют оксидазный тест любым из методов (наложением мембранных фильтров на диск фильтровальной бумаги, смоченной реактивом, нанесением штрихом культуры на полоску фильтровальной бумаги, смоченной реактивом, накапыванием реактива на колонию и другими). При изменении цвета всех колоний (оксидазоположительные) дают отрицательный ответ.
Не изменившие цвета после контакта с реактивом типичные колонии подсчитывают и относят к группе ОКБ.
Второй вариант
Подсчитывают число типичных колоний каждого типа и подтверждают их способность образовывать кислоту и газ путем посева на полужидкую среду с глюкозой. Исследуют не менее 2 - 3 колоний каждого типа. Посевы инкубируют при температуре 37 °С. Просмотр реакции проводят через 4 - 6 часов и при наличии кислоты и газа дают положительный ответ. Пробирки, где образовалась только кислота или среда не изменилась, оставляют для окончательного учета через 24 часа.
К группе ОКБ относят бактерии, образующие типичные колонии на среде Эндо и кислоту и газ при ферментации глюкозы.
Допускается использование любых тест-систем для установления способности газообразования при ферментации углевода, имеющие сертификат качества.
Примечание. При производственном контроле наличие ОКБ служит основанием к приостановке выдачи сертификата качества на данную партию продукции. Дальнейшую идентификацию выросших розовых колоний можно не продолжать.
Определение глюкозоположительных колиформных бактерий методом мембранной фильтрации
В индикаторную группу ГКБ входят помимо ОКБ еще и лактозоотрицательные бактерии семейства Enterobacteriaceae, оксидазоотрицательные, растущие на среде Эндо в виде разного типа розовых колоний, ферментирующие глюкозу до кислоты и газа при температуре (37 ± 1) °С.
Принцип метода определения ГКБ заключается в подтверждении наличия бактерий, ферментирующих глюкозу до кислоты и газа в том же посеве, что и для определения ОКБ. При обнаружении типичных и розовых (или только розовых) колоний подсчитывают ОКБ, а затем продолжают идентификацию розовых колоний по оксидазному тесту и способности образования кислоты и газа на подтверждающих средах с глюкозой.
Выполнение анализа
Если на фильтрах помимо типичных выросли колонии, характерные для лактозоотрицательных бактерий семейства Enterobacteriaceae - розовые, розовые с красным центром, бледно-розовые, белесые (или только лактозоотрицательные), выполняют оксидазный тест путем помещения мембранного фильтра на кружок фильтровальной бумаги, обильно смоченный реактивом для оксидазного теста. При признаках проявления реакции, но не позднее, чем 5 минут, фильтр переносят обратно на среду Эндо и учитывают результат после четкого проявления реакции.
Если все колонии изменили цвет (оксидазоположительные), дают отрицательный ответ.
При наличии колоний, не изменивших цвет (оксидазоотрицательных), подсчитывают число таких колоний каждого типа и производят пересев в полужидкие среды с глюкозой. Исследуют не менее 2 - 3 колоний каждого типа. Инкубируют посевы при 37 °С в течение 4 - 24 часов. В качестве ОКБ подсчитывают типичные колонии. В качестве ГКБ подсчитывают в сумме колонии как типичные, так и розовые, которые способны образовывать кислоту и газ при ферментации глюкозы.
Учет результатов анализа при определении общих и глюкозоположительных колиформных бактерий
При отсутствии роста на мембранных фильтрах или при отрицательном ответе в подтверждающих тестах в протоколе анализа указывают: ОКБ и ГКБ не обнаружены в 300 мл.
При росте на фильтрах типичных колоний лактозоположительных бактерий и подтверждении их принадлежности к группе ОКБ (либо с отрицательным оксидазным тестом, либо ферментирующих глюкозу до кислоты и газа) их число суммируют, сумму делят на три и в протоколе анализа указывают: число КОЕ ОКБ/100 мл; и число КОЕ ГКБ/100 мл. В данном случае результаты по ОКБ и ГКБ - одинаковые, поскольку ОКБ ферментируют как лактозу, так и глюкозу до кислоты и газа.
При росте на фильтрах помимо типичных еще и розовых колоний оксидазоотрицательных бактерий, а также только розовых, подсчитывают число колоний, ферментирующих глюкозу до кислоты и газа при температуре 37 °С, затем суммируют с числом ОКБ, делят на три. В протоколе анализа указывают результат: число КОЕ ГКБ/100 мл.
Обнаружение оксидазоположительных колоний служит показанием к проведению анализа на обнаружение Ps. aeruginosa.
Определение общих и глюкозоположительных колиформных бактерий титрационным методом
Ускорение анализа достигают использованием на первом этапе анализа в качестве среды накопления глюкозопептонной среды. Этот прием позволяет в одном посеве определять ОКБ и ГКБ, что возможно благодаря способности ОКБ ферментировать как лактозу, так и глюкозу, как основной биохимический признак семейства Enterobacteriaceae. Кроме того накопление колиформных бактерий в среде с глюкозой происходит более интенсивно за счет быстрого разложения глюкозы по сравнению с лактозой, что сокращает время анализа на сутки.
Выполнение анализа
Глюкозопептонную среду готовят также, как лактозопептонную, заменив углевод лактозу на глюкозу МУК 4.2.1018-01.
Исследуемый объем воды 300 мл засевают в три емкости с 10 мл концентрированной глюкозопептонной среды по 100 мл в каждую емкость. Посевы инкубируют при температуре (37 ± 1) °С в течение 24 часов.
Отсутствие изменения среды позволяет дать отрицательный ответ.
Из посевов в среду накопления, где отмечено помутнение и газообразование или только помутнение производят высев на сектора среды Эндо с таким расчетом, чтобы получить изолированные колонии. Посевы на среде Эндо инкубируют при температуре (37 ± 1) °С в течение 16 - 18 часов.
При обнаружении роста на секторах характерных для колиформных бактерий колоний выполняют оксидазный тест одним из способов (нанесением штрихом колонии каждого типа на полоску фильтровальной бумаги, смоченной реактивом; нанесением капли реактива на часть сектора).
Отрицательный ответ дают в следующих случаях:
• в среде накопления нет признаков роста;
• на секторах среды Эндо нет роста;
• на секторах среды Эндо выросли не характерные для колиформных бактерий колонии (прозрачные, с неровными краями, расплывчатые);
• все колонии на секторе оказались оксидазоположительные.
В протоколе анализа сообщают: отсутствие ОКБ в 300 мл и отсутствие ГКБ в 300 мл.
При обнаружении на секторах роста типичных оксидазоотрицательных колоний - темно-красных, красных, с металлическим блеском или без него дают ответ о наличии ОКБ и ГКБ в пробе воды. В протоколе анализа сообщают: обнаружение ОКБ в 300 мл, обнаружение ГКБ в 300 мл.
Если на секторах не выявлен рост типичных колоний, а обнаружены розовые оксидазоотрицательные колонии и при этом в среде накопления установлено газообразование - дают ответ о наличии ГКБ. В протоколе анализа сообщают: обнаружение ГКБ в 300 мл.
Данный анализ является качественным. При необходимости получения количественного результата производят посев в глюкозопептонную среду трех объемов по 100 мл, трех объемов по 10 мл и трех объемов по 1 мл и устанавливают в каждой емкости наличие ОКБ и ГКБ, как указано выше.
При определении ОКБ учитывают емкости, при высеве из которых на среде Эндо обнаружены типичные колонии.
При определении ГКБ учитывают в сумме емкости, где на секторах среды Эндо обнаружены типичные колонии ОКБ, а также розовые, при газообразовании в среде накопления выдают ответ: НВЧ КОЕ ОКБ в 100 мл или НВЧ КОЕ ГКБ в 100 мл.
Результаты определяют по таблице МУК 4.2.1018-01.
Примечания.
В соответствии с СанПиН единицей измерения ОКБ ГКБ и ТКБ является 100 мл, а норматив по этим показателям - отсутствие колиформных бактерий в 300 мл.
Норматив - это научно обоснованная величина, указывающая (при его соблюдении) на вероятность обеспечения эпидемической безопасности водопользования в отношении кишечных инфекций.
Единица измерения 100 мл условно принята для выражения количественного результата в целях сопоставления данных на международном уровне, а также при исследовании воды различных объектов и при работе разными методами (мембранным или титрационным). При работе итерационным методом результат может быть высчитан только на 100 мл в соответствии с международными статистическими таблицами расчета НВЧ (наиболее вероятного числа) микроорганизмов.
Приложение 9
Метод определения Pseudomonas aeruginosa
Приготовление питательных сред.
Среда Бонде.
Натрий лимоннокислый трехзамещенный 28 г;
Натрий-аммоний фосфорнокислый 15 г;
Калий фосфорнокислый однозамещенный 10 г;
Магний сернокислый (сульфат магния) 2 г;
Вода дистиллированная 1000 мл.
Ингредиенты растворяют при нагревании, стерилизуют при 1 атм. 20 мин. Перед посевом добавляют 5 мл 0,01 %-ного водного раствора кристаллического фиолетового на 100 мл среды.
Среда «Блеск»
100 мл питательного агара, стерильного, приготовленного из сухого препарата по прописи на этикетке, расплавляют на водяной бане. После охлаждения до температуры (приблизительно) 50 °С добавляют 0,3 г L-аргинина, 8 мл 10 %-ного водного раствора трифенилтетразолий хлорида (ТТХ), 10 мл стерильного обезжиренного теплого молока, тщательно перемешивают и разливают в чашки не тонким слоем (не менее 25 мл).
Выполнение анализа
Исследуют пробу воды объемом 1000 мл, разделенную в две емкости по 500 мл. В каждую емкость добавляют по 50 мл среды Бонде, тщательно перемешивают и инкубируют при температуре (37 ± 1) °С в течение 24 - 48 часов.
Через 24 часа просматривают посевы. При наличии роста Pseudomonas aeruginosa происходит помутнение среды Бонде и на поверхности появляется тонкая прозрачная пленка, часто поднимающаяся по стенке емкости. В журнале отмечают помутнение среды и образование пленки.
Для подтверждения Pseudomonas aeruginosa делают посев на среду «Блеск». Емкость перед посевом не взбалтывать. Петлей забирают пленку и делают посев штрихом для получения изолированных колоний и по 3 - 4 бляшки из каждой емкости. Посев в виде бляшки: Делают укол петлей до дна чашки и затем растирают небольшую площадку вокруг укола по поверхности среды. Допустимо делать посев нескольких проб на секторах одной чашки. Посевы со средой «Блеск» инкубируют при температуре (37 ± 1) °С в течение 24 часов.
Емкости со средой Бонде оставляют в термостате еще на 24 часа для окончательного учета.
Через 24 часа отмечают характер роста на среде «Блеск». При наличии в пробе Ps. aeruginosa на среде «Блеск» вырастают темно-красные колонии с золотистым блеском или золотистыми вкраплениями на «бляшках». Появление блеска можно наблюдать уже через 20 - 22 часа инкубации при температуре 37 °С, но максимального развития реакция достигает через 42 - 44 часа.
Если на среде «Блеск» не отмечено роста или выросли колонии темно-красные, темно-вишневые, но без характерного блеска, то из емкостей, где отмечено помутнение или помутнение с пленкой, высев следует повторить через 48 часов.
При отсутствии роста в среде Бонде через 24 часа пробу инкубируют до 48 часов и в случае помутнения и образования пленки подтверждают Ps. aeruginosa на среде «Блеск», как указано выше.
Подтвердить наличие Ps. aeruginosa также можно путем посева подозрительной изолированной колонии на косяк с питательным агаром, на котором через 24 часа инкубации при температуре 37 °С в случае положительной реакции появляется синий, сине-зеленый, зелено-желтый пигмент. Пигментация может усиливаться при последующем выдерживании косяка на свету при комнатной температуре.
Отрицательный ответ выдают:
• при отсутствии признаков роста в посевах пробы в среду Бонде;
• при отсутствии роста на среде «Блеск»;
• при росте на среде «Блеск» не характерных для Ps. aeruginosa колоний без блеска.
Результат сообщают: Ps. aeruginosa не обнаружена в 1000 мл воды.
Положительный ответ выдают:
• при росте на среде «Блеск» темно-красных колоний с золотистым блеском;
• при образовании характерного пигмента на питательном агаре.
При четкой реакции на среде Бонде (муть и пленка) и среде «Блеск» наличие пигмента определять не обязательно.
Результаты вносят в протокол анализа: Ps. aeruginosa обнаружена в 1000 мл воды.
Приложение 10
(обязательное)
Метод определения колифагов в воде
Принцип метода определения колифагов
Метод заключается в предварительном размножении колифагов в среде обогащения в присутствии Е. coli и последующем его выявлении в виде зон лизиса (просветления) на газоне Е. coli на питательном агаре.
Выполнение анализа при определении колифагов
Подготовка посуды, питательных сред (питательный агар готовят по способу, указанному на этикетке), мембранных фильтров, ведение культуры Е. coli, методика подтверждения фаговой природы лизиса выполняется на МУК 4.2.1018-01.
Накануне проведения анализа культуру Е. coli засевают в две пробирки со скошенным агаром. Через 18 ± 2 ч инкубации при температуре 37 ± 1 °С производят смыв бактерий с косяков 5 мл стерильного физиологического раствора и по стандарту мутности готовят взвесь Е. coli в концентрации 109 бактериальных клеток в мл.
В исследуемую воду объемом 1000 мл вносят 100 мл 10-кратного питательного бульона и 10 мл смыва Е. coli. Для контроля культуры 0,1 мл смыва Е. coli помещают в чашку Петри и заливают питательным агаром.
Подготовленную пробу воды и чашку Петри с контролем Е. coli помещают в термостат и инкубируют при температуре 37 ± 1 °С в течение 18 ± 2 ч.
После инкубации, при отсутствии колифагов на контрольной чашке, в стерильную пробирку отливают 10 мл и эту пробу освобождают от бактериальной флоры одним из двух методов.
1. В 10 мл пробы добавляют 1 мл хлороформа, пробирку закрывают стерильной резиновой или силиконовой пробкой, энергично встряхивают в течение 3 - 5 минут для равномерного распределения хлороформа по объему пробы и оставляют на 15 минут при комнатной температуре для полного осаждения хлороформа. Для дальнейшего исследования отбирают 1 мл пробы, не касаясь хлороформа.
2. 10 мл пробы фильтруют через мембранный фильтр с размером пор 0,45 мм, подготовленный по п. 7.1 МУК 4.2.1018-01.
Фильтрат в объеме 1 - 2 мл отбирают в стерильную пробирку, помещенную в колбу Бунзена или непосредственно в стерильную колбу Бунзена. Полученный фильтрат используют для дальнейшего исследования.
В предварительно расплавленный и остуженный до 45 °С питательный агар добавляют приготовленный смыв бактерий Е. coli из расчета 1,0 мл смыва на 100 мл агара. В стерильную чашку Петри пипеткой переносят 1 мл пробы освобожденной от сопутствующей бактериальной флоры одним их двух предложенных методов. Сверху пробу заливают подготовленным агаром. В качестве контроля Е. coli дополнительно заливают одну стерильную чашку Петри. Залитые чашки осторожно покачивают для равномерного распределения агара. После застывания агара чашки переворачивают и помещают в термостат на 18 ± 2 ч при 37 ± 1 °С.
Если исследуется несколько проб, то целесообразно использовать одну чашку Петри, которую необходимо залить агаром с Е. coli. После застывания агара разделить его поверхность на сектора (не более 6), пронумеровать их согласно количеству исследованных проб. На каждый сектор нанести каплю микропипеткой или штрихом стерильной бактериологической петлей из исследуемой пробы воды, оставив один сектор в качестве контроля.
Учет результатов
Просмотр чашек после инкубирования осуществляется в проходящем свете. Проба считается положительной при наличии полного лизиса газона Е. coli, наличии отдельных зон лизиса или единичных бляшек на чашке с исследуемой пробой воды при отсутствии зон лизиса или отдельных бляшек на контрольной чашке или контрольном секторе.
В протоколе отмечается: колифаги обнаружены или не обнаружены в 1000 мл воды.
При наличии зон лизиса в контроле результат считается недействительным. Анализ следует повторить с новой культурой Е. coli.
Приложение 11
(обязательное)
Контроль за содержанием ооцист криптоспоридий в воде
Очищенная вода не должна содержать ооцист криптоспоридий. Исследование проводят в соответствии с МУК 4.2.964-00 (п. 2.1). Далее полученный осадок распределяют равномерно на предметных стеклах (не менее 4) и высушивают на воздухе. На тщательно высушенный мазок наносят 2 - 3 капли смеси Никифорова (смесь равных частей серного эфира и 96° этилового спирта) на 8 - 12 минут. После чего предметные стекла ставят вертикально и тщательно высушивают.
После этого мазки быстро проводят над пламенем горелки и окрашивают карболовым фуксином (см. раздел 4.3) в течение не менее 20 минут. Мазки промывают дистиллированной водой, обесцвечивают (дифференцируют) 5 - 10 %-ной серной кислотой в течение 10 - 20 секунд и снова промывают. Затем дополнительно окрашивают 0,2 %-ным водным раствором метиленового синего или 5 % малахитовой зелени в 10 % этиловом спирте в течение 3 - 5 минут. Промывают дистиллированной водой, тщательно высушивают на воздухе и исследуют с масляной иммерсионной системой микроскопа с увеличением не менее 1000х.
Ооцисты криптоспоридий окрашиваются в разные оттенки ярко-красного (малинового, вишневого) цвета и имеют вид округлых образований диаметром 5 - 6 микрон с отчетливо видимой оболочкой и структурированным содержимым (можно наблюдать наличие 4 веретенообразных темно-окрашенных спорозоитов) на синем или зеленом основном фоне.
Приложение 12
(рекомендуемое)
Схема микробиологического контроля на различных этапах производства расфасованной воды (при сокращенном анализе в каждой партии и сокращенном периодическом анализе)
|
№ п.п. |
Места отбора |
Показатели |
Периодичность отбора проб |
|
1 |
Исходная вода |
ОМЧ при температуре 37 °С |
1 раз в неделю |
|
Колиформы* |
|||
|
Pseudomonas aeruginosa** |
1 раз в месяц |
||
|
Клостридии*** |
|||
|
2 |
Накопительный резервуар до водоподготовки |
ОМЧ при 37 °С и 22 °С |
1 раз в неделю |
|
Колиформы* |
|||
|
3 |
Каждый этап водоподготовки |
ОМЧ при 37 °С |
1 раз в неделю |
|
4 |
После очистки и обеззараживания |
ОМЧ при 37 °С |
1 раз в неделю |
|
Колиформы* |
|||
|
5 |
Готовая продукция перед розливом с каждой линии |
ОМЧ при 37 °С |
1 раз в сутки |
|
Колиформы* |
|||
|
ОМЧ при 22 °С |
1 раз в неделю |
||
|
Pseudomonas aeruginosa** |
1 раз в месяц |
||
|
Клостридии*** |
|||
|
6 |
Емкости (одноразовые) Смыв с 10 бутылок до 2 л Смыв с 4 бутылок 5 л |
ОМЧ при 37 °С Колиформы |
1 раз в сутки |
|
7 |
Емкости возвратные с каждой автоматической моечной машины |
ОМЧ при 37 °С |
2 раза в месяц |
|
Колиформы |
|||
|
8 |
Емкости возвратные после ручной мойки |
ОМЧ при 37 °С |
2 раза в неделю |
|
Колиформы |
|||
|
9 |
Укупорочные изделия |
ОМЧ при 37 °С Колиформы |
1 раз в неделю |
|
10 |
Расфасованная готовая продукция через 5 дней хранения |
ОМЧ при 37 °С и 22 °С |
1 раз в неделю |
|
Колиформы* |
|||
|
Pseudomonas aeruginosa** |
|||
|
11 |
Расфасованная готовая продукция через 1 месяц хранения |
ОМЧ при 37 °С и 22 °С |
1 раз в месяц |
|
Колиформы* |
|||
|
Pseudomonas aeruginosa** |
|||
|
Примечания. 1. * Колиформы - общие и глюкозоположительные колиформные бактерии. 2. ** Pseudomonas aeruginosa определяет лаборатория, находящаяся вне территории производства; при обнаружении ОМЧ свыше допустимых норм. 3. *** Споры сульфитредуцирующих клостридий определяют при использовании воды поверхностного источника (автономного или централизованного) водоснабжения или из незащищенного и малозащищенного водоносного горизонта (подрусловые, грунтовые воды, фильтрационные). 4. На производствах, где обеззараживание проводят на заключительном этапе водоподготовки непосредственно перед розливом, пункты 4 и 5 совпадают. 5. Пункты 5, 10, 11 относятся к каждому виду готовой продукции. 6. Частота контроля, указанная в пунктах 5, 10, может быть сокращена для производств с выпуском не более 100 бутылок в смену. По пунктам 10 и 11: отбор проб производится 1 раз в неделю (1 раз в месяц) из емкостей, отобранных на хранение, методом случайной выборки. |
|||
Приложение 13
(обязательное)
Методика бактериологического контроля емкостей и укупорочных изделий
Бактериологический контроль производят по двум показателям: ОМЧ и колиформы
1. Метод бактериологического контроля одноразовых емкостей
Для исследования берут 10 емкостей объемом 2,0 л и менее или 4 емкости объемом 5,0 л. Выборку емкостей осуществляет сотрудник лаборатории из каждой партии, используемой для розлива, 1 раз в неделю. Горлышко каждой бутыли должно быть закрыто стерильной фольгой.
Смывы с бутылок производят в лаборатории после обработки помещения бактерицидными лампами.
Смывы выполняет путем последовательного перелива 100 мл стерильного физиологического раствора (8,5 %-ного хлористого натрия) из одной бутылки в другую после тщательного ополаскивания всей внутренней поверхности емкостей.
Из последней емкости делают посев по 1 мл смывной жидкости параллельно в 2 чашки Петри, заливают посевы 8 - 10 мл расплавленного и охлажденного до температуры 45 °С градусов питательного агара по общепринятой методике. Посевы инкубируют при температуре 37 °С в течение 24 - 48 часов.
Оставшуюся жидкость профильтровывают через мембранный фильтр с диаметром пор 0,45 мкм, помещают на среду Эндо или засевают в глюкозопептонную среду накопления при работе титрационным методом. Посевы инкубируют при температуре 37 °С и определяют колиформные бактерии по методике приложения 9.
Емкости могут считаться годными для розлива при отсутствии колиформных бактерий и обнаружении не более 2 КОЕ/мл ОМЧ.
2. Метод бактериологического контроля возвратных емкостей
Для исследования выбирают по 2 емкости с каждой автоматической моечной машины 2 раза в месяц. Емкости закрывают стерильной фольгой и переносят в лабораторию.
Для определения ОМЧ сливают остаточную промывную воду в стерильную посуду с соблюдением правил стерильности. Посев остаточной воды производится как описано в методе 1 для сливной жидкости.
Для определения колиформ в одну из емкостей наливают 100 мл стерильного физиологического раствора, тщательно ополаскивают внутреннюю поверхность, переливают во вторую и после ополаскивания фильтруют через мембранный фильтр как описано в методе 1. При ручной мойке емкостей посев производят 2 раза в неделю.
3. Метод бактериологического контроля укупорочных изделий
Бактериологический контроль укупорочных изделий производят не реже 1 раза в месяц.
Изделия, предназначенные для укупорки одноразовых емкостей, отбирают стерильным пинцетом в количестве 10 штук в стерильную широкогорлую колбу, заливают 100 мл стерильного физиологического раствора и встряхивают в течение 5 мин. Определение ОМЧ производят как описано в методе 1. Оставшуюся жидкость фильтруют для определения колиформ.
Изделия, предназначенные для возвратных емкостей, также отбирают стерильным пинцетом непосредственно перед укупоркой в количестве 4 штук. С помощью стерильного тампона, смоченного в 10 мл физиологического раствора, производят смыв с внутренних поверхностей последовательно всех 4 изделий, периодически смачивая тампон. Затем тампон тщательно встряхивают в течение 5 минут в этом же физиологическом растворе, отжимают вращательным движением, прижимая к стенкам пробирки и удаляют. Производят посев на ОМЧ методом заливки, на колиформы - методом мембранной фильтрации как это описано в методе 1.
Укупорочные изделия считаются пригодными при отсутствии колиформных бактерий и при обнаружении не более 2 КОЕ/мл ОМЧ.
Приложение 14
(обязательное)
Контроль качества ополаскивания возвратных емкостей
Контроль качества ополаскивания возвратных емкостей, т.е. контроль на наличие остатка моющих средств, производят по изменению рН в воде остающейся в емкостях после ополаскивания.
При использовании каустических (щелочных) препаратов контроль проводят индикатором - 0,5 % фенолфталеином. Для этого остаточную воду из емкости сливают в чистую посуду и добавляют 1 - 2 капли фенолфталеинового индикатора. Окрашивание воды в розовый цвет указывает на наличие каустического моющего средства в емкостях, что требует повышения длительности и интенсивности ополаскивания.
При использовании для мытья емкостей моющих средств, не содержащих каустических соединений, качество промывки емкостей определяют по разнице рН в воде, используемой для ополаскивания, и в воде оставшейся емкости.
Если рН воды из вымытой емкости меньше, чем рН промывной воды, то это является доказательством присутствия моющего некаустического средства и основанием для требования проведения мероприятий по улучшению этого этапа производства расфасованной воды.
|
|